Hapokkuuden ja emäksisyyden Brønsted-Lowry-määritelmä
Aloitamme keskustelun happo-emäskemiasta parilla keskeisellä määritelmällä. Ensimmäisen näistä ehdottivat tanskalainen kemisti Johannes Brønsted ja englantilainen kemisti Thomas Lowry vuonna 1923, ja se on tullut tunnetuksi happamuuden ja emäksisyyden Brønsted-Lowry-määritelmänä. Brønstedin ja Lowryn määritelmän mukaan happo on laji, joka toimii protonien luovuttajana, kun taas emäs on protonien vastaanottaja. Olemme jo edellisessä luvussa käsitelleet yhtä tutuimmista esimerkeistä Brønsted-Lowryn happo-emäsreaktiosta, suolahapon ja hydroksidi-ionin välistä:
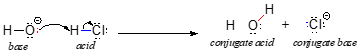
Tässä reaktiossa protoni siirtyy HCl:stä (happo eli protoninluovuttaja) hydroksidi-ioniin (emäs eli protonin hyväksyjä). Kuten edellisessä luvussa opimme, kaarevat nuolet kuvaavat elektronien liikkumista tässä sidoksia rikkovassa ja muodostavassa prosessissa.
Kun Brønsted-Lowry-happo luovuttaa protonin, jäljelle jäävää kutsutaan konjugaattiemäkseksi. Kloridi-ioni on siis suolahapon konjugaattiemäs. Kääntäen, kun Brønsted-Lowryn emäs ottaa vastaan protonin, se muuttuu konjugoituneeseen happomuotoonsa: vesi on siis hydroksidi-ionin konjugoitunut happo.
Tässä on orgaaninen happo-emäsreaktio etikkahapon ja metyyliamiinin välillä:
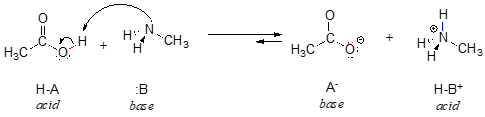
Tämän reaktion käänteisreaktiossa asetaatti-ioni on emäs ja metyyliammoniumioni (protonoitunut metyyliamiini) on happo.
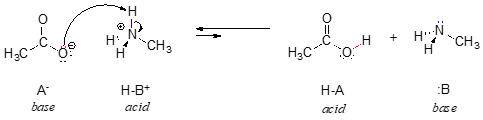
Mikä tekee yhdisteestä happaman (todennäköisesti luovuttaa protonin) tai emäksisen (todennäköisesti ottaa protonin)? Tähän kysymykseen vastaaminen on yksi tämän luvun tärkeimmistä tehtävistämme, ja se vaatii meitä käyttämään paljon siitä, mitä opimme orgaanisesta rakenteesta kahdessa ensimmäisessä luvussa, sekä termodynamiikkaa koskevia ajatuksia, joita tarkastelimme luvussa 6.
Pohditaan nyt vain yhtä emästen yhteistä ominaisuutta: toimiakseen emäksenä molekyylillä on oltava reaktiivinen elektronipari. Kaikissa happo-emäsreaktioissa, joita näemme tässä luvussa, emäksisellä lajilla on atomi, jolla on yksinäinen elektronipari. Kun esimerkiksi metyyliamiini toimii emäksenä, typpiatomin yksinäistä elektroniparia käytetään uuden sidoksen muodostamiseen protonin kanssa.
Metyyliammoniumioni ei selvästikään voi toimia emäksenä – sillä ei ole reaktiivista elektroniparia, jolla se voisi ottaa vastaan protonin.
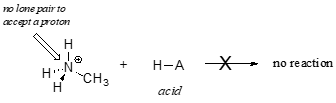
Myöhemmin luvussa 14 tutkimme reaktioita, joissa alkeenin tai aromaattisen renkaan sidoksessa oleva elektronipari toimii emäksisesti – mutta nyt keskitytään ei-sitoutuvien (yksinäisen parin) elektronien emäksisyyteen.
Harjoitus \(\PageIndex{1}\)
Toteuta alla olevat reaktiot – toisin sanoen piirrä rakenteet puuttuville konjugaattihapoille ja konjugaattiemäksille, jotka johtuvat annetuista kaarevista nuolista.