Introduction
Farbstoffsensibilisierte Solarzellen (DSCs) haben in den letzten Jahren viel Aufmerksamkeit auf sich gezogen, und zwar aufgrund ihrer guten photovoltaischen Leistung, insbesondere bei schwachem Licht, sowie ihrer Flexibilität in Bezug auf Farben und Aussehen, ihrer relativ einfachen Herstellungsverfahren und ihrer potenziell niedrigen Kosten. Effiziente Farbstoffsolarzellen (DSC) wurden erstmals in den 1990er Jahren durch die bahnbrechende Arbeit von O’Regan und Grätzel (1991) entwickelt, die erstmals mesoporöse TiO2-Elektroden verwendeten, die aus kolloidalen TiO2-Nanopartikeln hergestellt wurden (O’Regan und Grätzel, 1991).
Der Funktionsmechanismus von DSC unterscheidet sich stark von anderen Arten von Solarzellen (O’Regan und Grätzel, 1991; Hagfeldt et al., 2010). In ihrem ursprünglichen Konzept ist die DSC eine photoelektrochemische Solarzelle, die aus einer farbstoffsensibilisierten mesoporösen TiO2-Arbeitselektrode (WE), einem Redox-Elektrolyten und einer Gegenelektrode (CE) besteht. Sowohl die WE als auch die CE können (halb)transparent sein, so dass die Solarzelle von beiden Seiten beleuchtet werden kann. Farbstoffmoleküle, die mit geeigneten Verankerungsgruppen versehen sind, werden als Monoschicht auf der mesoporösen TiO2-Elektrode adsorbiert. Wenn die Farbstoffe Licht absorbieren, können die angeregten Moleküle Elektronen in das Leitungsband von TiO2 injizieren (Elektronentransfer (ET) Reaktion 1 in Abbildung 1). Ein Redox-Mediator im Elektrolyten regeneriert die entstandenen oxidierten Farbstoffmoleküle (ET 2). Die oxidierte Form des Mediators ist für den Transport der positiven Ladung zur Gegenelektrode durch Diffusion verantwortlich. Schließlich werden Elektronen im TiO2 auf dem darunter liegenden, mit Fluor-dotiertem Tinoxid (FTO) beschichteten Glassubstrat gesammelt und wandern durch einen externen Kreislauf zur Gegenelektrode, wo sie den oxidierten Redox-Mediator reduzieren (ET 3), wodurch sich der Kreislauf schließt. Eine schematische Darstellung dieser Prozesse ist in Abbildung 1 zu sehen.
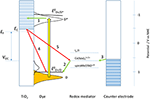
Abbildung 1. Energieschema und Funktionsmechanismus einer Farbstoffsolarzelle. Elektronentransferreaktionen sind mit Zahlen und Pfeilen (grün für Vorwärtsbewegung, rot für Rekombination) gekennzeichnet, auf die im Text Bezug genommen wird. Die Energieniveaus verschiedener Redox-Mediatoren sind angegeben (Spiro-MeOTAD ist ein Festkörper-Lochleiter).
Eine Reihe von Rekombinationsreaktionen in der DSC konkurrieren mit den oben beschriebenen Vorwärtsprozessen. Die strahlende und nicht-strahlende De-Anregung des Farbstoffs konkurriert mit der Elektroneninjektion aus dem angeregten Farbstoff in das Leitungsband von TiO2. Darüber hinaus können die Elektronen im TiO2 mit oxidierten Farbstoffmolekülen (ET 4) oder mit der oxidierten Form des Redox-Mediators (ET 5) rekombinieren. Bei optimierten DSC-Systemen liegt die Umwandlungseffizienz von einfallenden Photonen in Strom (IPCE) bei etwa 90 %. Da es einige Reflexions- und Transmissionsverluste gibt, bedeutet dies, dass jedes absorbierte Photon unter den verwendeten Messbedingungen, typischerweise unter Kurzschlussbedingungen, ein Elektron im externen Stromkreis erzeugt. Unter Betriebsbedingungen, wenn die Solarzelle ihre maximale Leistung abgibt (im Punkt maximaler Leistung, MPP), ist die IPCE deutlich niedriger und es treten sowohl Strom- als auch Spannungsverluste auf. Um die DSC vollständig zu optimieren, müssen diese Verluste minimiert werden, wie im Abschnitt Begrenzende Faktoren in der DSC erörtert wird.
Das Redoxpaar Triiodid/Iodid (I3-/I-) wird am häufigsten in DSCs verwendet. Dieses komplexe Redoxpaar hat jedoch einige schwerwiegende Einschränkungen, wie in unserer früheren Arbeit (Boschloo und Hagfeldt, 2009) aufgezeigt wurde. Insbesondere ist sein formales Reduktionspotenzial (E0′) relativ negativ (+0,35 V gegen NHE) im Vergleich zum E0′ (D+/D) typischer Farbstoffe (bei ca. 1 V gegen NHE), was zu einem großen Verlust von mehr als 0,5 V führt. Der Grund dafür liegt in dem mehrstufigen Regenerationsmechanismus, der die Bildung des I2-Radikals als Reaktionszwischenprodukt beinhaltet. Außerdem ist Triiodid ziemlich stark gefärbt und es gibt Probleme mit der Langzeitstabilität (Partikel). Kurz gesagt, Triiodid/Iodid ist nicht der Weg zu einer DSC mit höherer Leistung. Mehrere vielversprechende alternative Redox-Mediatoren werden in Abschnitt Komponenten für effizientere DSCs diskutiert.
Ein Nachteil gegenüber anderen Solarzellentechnologien ist die Verwendung eines flüssigen Redox-Elektrolyten in effizienten DSCs. Dadurch wird die Verkapselung problematisch und die Geräte sind weniger kompatibel mit anderen Festkörper-Photovoltaiktechnologien. Der flüssige Redoxelektrolyt kann jedoch durch einen Festkörper-Lochleiter in DSCs ersetzt werden, um DSCs in Festkörpertechnik herzustellen (Bach et al., 1998). Leider geht dies in der Regel mit einer schnelleren Rekombination und einer geringeren Gesamtleistung einher.
Um einen signifikanten Einfluss auf den Bereich der Photovoltaik zu haben, muss die Leistung von DSC weiter verbessert werden. Ihre Rekordwirkungsgrade bei einer Sonneneinstrahlung (siehe Tabelle 1) liegen knapp über 10 % und damit unter denen der meisten anderen konkurrierenden Photovoltaiktechnologien. Bei Innenraumanwendungen hält DSC jedoch mit 32 % bei 1.000 Lux den Leistungsrekord (Cao et al., 2018). Ein Grund dafür ist, dass das Absorptionsspektrum des Farbstoffs ideal mit dem Emissionsspektrum einer Innenraum-Lichtquelle übereinstimmen kann.
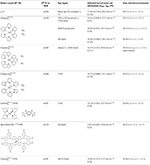
Tabelle 1. Redox-Mediatoren und Farbstoffe, die in Hochleistungs-Farbstoffsolarzellen verwendet werden.
Dieser Blickwinkel konzentriert sich vor allem auf die Effizienz von DSCs, aber letztlich ist ihre Langzeitstabilität für praktische Anwendungen ebenso wichtig.
Begrenzende Faktoren in der DSC
Die Shockley-Queisser (SQ)-Grenze gibt den maximal erreichbaren Wirkungsgrad für ein photovoltaisches Gerät mit einem Übergang an, der bei einer Sonneneinstrahlung von 1.000 W m-2 und einer AM1,5G-Spektralverteilung 33,8 % beträgt (Green, 2012). Dieser Grenzwert wurde zwar für Halbleiterbauelemente abgeleitet, gilt aber im Prinzip auch für DSCs. Die Bandlücke Eg legt den Bereich für die Lichtabsorption fest: Alle Photonen mit Energien größer als Eg werden absorbiert und tragen zum Photostrom bei, diejenigen mit kleineren Energien werden durchgelassen und nicht genutzt. Die einzigen Rekombinationsprozesse, die bei der Herleitung der SQ-Grenze berücksichtigt werden, sind strahlende Prozesse, da diese unvermeidlich sind. Alle nicht-strahlenden Rekombinationsprozesse senken den Wirkungsgrad weiter. Nach der SQ-Analyse liegt die optimale Bandlücke bei 1,3 eV; die maximal erreichbare Effizienz sinkt allmählich auf 25 % für Eg = 1,9 eV. Dies entspräche einem Farbstoff mit einer Wellenlänge des Absorptionsbeginns von 650 nm, ein Wert, der üblicherweise für effiziente Sensibilisierungsfarbstoffe in der DSC ermittelt wird. Der entsprechende theoretische Photostrom unter Kurzschlussbedingungen, JSC, würde 17 mA cm-2 betragen.
Während das maximale Leerlaufpotential (VOC) in der Halbleiter-Photovoltaik Eg/e als absolute Obergrenze hat, wird bei der DSC die Obergrenze durch die Differenz zwischen dem Leitungsbandpotential EC des TiO2 auf der einen Seite und dem Redoxpotential des Elektrolyten auf der anderen Seite festgelegt. Dieser Wert wird immer kleiner sein als die „Bandlücke“ des Farbstoffs. Der EC-Wert von TiO2-Anatas liegt bei etwa -0,5 V gegen NHE, wenn seine Oberfläche ungeladen ist (d. h. bei neutralem pH-Wert, ohne spezifische Ionenadsorption und ohne Elektronenakkumulation). Dieses Niveau kann durch Zusätze im Elektrolyten verändert werden, die zu einer Änderung der Oberflächenladung führen oder das Dipolmoment an der Grenzfläche zwischen Halbleiter und Elektrolyt verändern. Alternativ kann das EC durch chemische Modifikation des TiO2 verändert werden, z. B. durch Einbau von Mg in die Struktur, wodurch das EC auf ein negativeres Potenzial verschoben werden kann, auf etwa -0,7 V gegenüber NHE (Kakiage et al., 2016). Hauchdünne Metalloxidschichten (z. B. Al2O3), die das mesoporöse TiO2 bedecken, können ebenfalls die Lage des EC beeinflussen (Kay und Grätzel, 2002). Solche Schichten wirken sich auch auf die Kinetik von Grenzflächen-Elektronentransferreaktionen aus und können zur Feinabstimmung der Eigenschaften der DSC verwendet werden.
Das elektrochemische Potential der Elektronen im TiO2, gewöhnlich als Fermilevel EF bezeichnet, ist gegeben durch:
wobei kB die Boltzmann-Konstante ist, T die absolute Temperatur, e die Elementarladung (kBT/e ist 0.0257 V bei Raumtemperatur), nc die Dichte der Elektronen im Leitungsband und Nc die effektive Dichte der elektronischen Zustände am unteren Ende des Leitungsbandes. Nc ist eine Materialkonstante und beträgt etwa 1020 cm-3 für TiO2-Anatas. Bei Beleuchtung im offenen Stromkreis hängt EF von nc ab, das wiederum vom Erzeugungsfluss der injizierten Elektronen und den Ratenkonstanten für die Elektronenrekombination abhängt. Als Faustregel gilt, dass EF bei 1 Sonne um etwa 0,1 V positiver ist als EC.
Die formalen Reduktionspotentiale einer Reihe von Redox-Mediatoren für DSC sind in Tabelle 1 zusammen mit den erzielten Aufzeichnungseffizienzen in DSCs aufgeführt. Anfängliche Arbeiten zu DSCs konzentrierten sich auf das I3-/I-Redoxpaar, das eine sehr günstige Elektronentransferkinetik aufweist, was zu sehr geringen Rekombinationsverlusten und hoher JSC führt. Dies geht jedoch auf Kosten einer relativ niedrigen VOC aufgrund des eher negativen Wertes des Redoxpotentials. Erfolgreiche alternative Redox-Mediatoren haben ein positiveres Redox-Potential und können höhere VOC liefern. Fast alle diese Redoxvermittler führen jedoch zu einer schnelleren Elektronenrekombination zu oxidierten Redoxvermittlern, wodurch das Fermi-Niveau auf dem TiO2 unter Betriebsbedingungen gesenkt wird.
Die höchste berichtete VOC für eine DSC beträgt 1,4 V und wurde für ein Mg-dotiertes TiO2 mit zusätzlicher Oberflächenmodifikation durch MgO und Al2O3, sensibilisiert durch einen Cumarin-Farbstoff, und in Kombination mit dem Redoxpaar Br3-/Br- erzielt (Kakiage et al., 2016). Durch die Dotierung und Oberflächenmodifikation des TiO2 wurde die Leitungsbandkante auf etwa -0,7 V gegenüber NHE angehoben, während das formale Potenzial des Redoxpaares bei etwa +0,9 V gegenüber NHE liegt.
Die leistungsfähigsten DSCs mit Co(bpy)3-Redoxelektrolyt erreichen eine VOC von etwa 0,9 V. Die VOC für die besten ssDSCs mit Spiro-MeOTAD-Lochleiter beträgt etwa 0,8 V. Da sich die Redoxpotentiale des Co- und des spiro:MeOTAD-Lochleiters um etwa 0,2 V unterscheiden, bedeutet dies, dass das Fermi-Niveau in TiO2 im mesoporösen TiO2 für das ssDSC-Gerät unter offenen Beleuchtungsbedingungen um etwa 0,3 eV niedriger ist. Dies ist auf die viel schnellere Rekombinationskinetik der Elektronen zurückzuführen. Unter Verwendung von Gleichung 1 kann geschätzt werden, dass die Konzentration der Leitungsbandelektronen in der ssDSC um viele Größenordnungen niedriger ist als in der Co(bpy)3-DSC.
Wie in Abbildung 1 dargestellt, zeigt das Energieniveau des Grundzustandsfarbstoffs eine Gaußsche Verteilung mit einer durchschnittlichen Energie, die um einen Betrag, der der Reorganisationsenergie λ entspricht, unter der formalen Redoxenergie liegt. Bei der Anregung sollten die Energieniveaus D* mit den Akzeptorniveaus im Leitungsband von TiO2 überlappen, um eine effiziente Elektroneninjektion zu ermöglichen. Ein niedrigerer Wert von λ würde eine bessere Übereinstimmung zwischen dem EC des Halbleiters und dem berechneten Standardpotential für den angeregten Farbstoff, E0(D+/D*), und einen geringeren Spannungsverlust in der DSC ermöglichen. Die Reorganisationsenergie des Farbstoffs ist auf die interne molekulare Reorganisation des Farbstoffs zurückzuführen, wenn er seinen Redoxzustand ändert, sowie auf die externe Reorganisation der Lösungsmittelhülle. Da kein Lösungsmittel vorhanden ist, sollten die Reorganisationsenergien in der Festkörper-DSC geringer sein.
Die Elektroneninjektion (Reaktion 1 in Abbildung 1) konkurriert mit strahlenden und nichtstrahlenden Zerfallsprozessen des angeregten Farbstoffs. Ein langlebiger angeregter Zustand des Farbstoffs ist daher günstig. Übermäßige Energieverluste während des Injektionsprozesses sollten jedoch vermieden werden (Haque et al., 2005). Nach der Injektion wandern die Elektronen durch den mesoporösen Film und werden auf dem FTO-Substrat gesammelt. Eine Rekombination der Elektronen zu oxidiertem Farbstoff (Reaktion 4) und der oxidierten Form des Redox-Mediators (Reaktion 5) muss vermieden werden. Die Elektronenlebensdauer ist der Kehrwert der Summe der Geschwindigkeitskonstanten der beiden Rekombinationsprozesse. Häufig wird davon ausgegangen, dass die Rekombination der Elektronen zum oxidierten Farbstoff vernachlässigbar ist, da die Regeneration des Farbstoffs in der Regel recht schnell im Mikrosekundenbereich erfolgt (Reaktion 3). Unter den Betriebsbedingungen der Solarzelle sammelt sich jedoch eine große Konzentration von Elektronen im mesoporösen TiO2 an, was den Rekombinationsprozess erheblich beschleunigt (Haque et al., 2000). Haque et al. stellten fest, dass die Halbwertszeit für die Rekombination zur Oxidation von Ru-Farbstoff (N3) auf etwa 1 ns sank, wenn ein Potenzial von -0,3 V gegen NHE an die mesoporöse TiO2-Elektrode angelegt wurde (Haque et al., 2000). Daher kann in der Farbstoffsolarzelle, die unter MPP-Bedingungen betrieben wird, eine erhebliche Rekombination zum oxidierten Sensibilisator stattfinden.
Die Kinetik der Elektronenrekombination zum Redoxelektrolyten hängt sehr stark von der Art der oxidierten Form des Redoxmediators ab. Sie ist sehr langsam bei Triiodid, schneller bei Kobaltvermittlern und noch schneller bei Vermittlern oder Lochleitern auf Triphenylaminbasis. Entscheidend für den erfolgreichen Einsatz der beiden letztgenannten ist, dass die Kinetik durch eine strukturelle Veränderung des Farbstoffs verlangsamt werden kann: Eine Gruppe kann den Rekombinationsprozess verlangsamen.
Eine lange Elektronenlebensdauer ist für die DSC von Vorteil, da sie die VOC verbessert. In normalen Flüssigelektrolyt-DSCs beträgt die Elektronenlebensdauer typischerweise 1-10 ms bei offenem Stromkreis und einer Sonnenbeleuchtung. Die Elektronentransportzeit sollte kleiner als die Lebensdauer sein, um Verluste während des Transports zu vermeiden. Typische Werte unter Kurzschlussbedingungen sind etwa eine Größenordnung kleiner als die Elektronenlebensdauer. Unter Betriebsbedingungen (bei MPP) ist der Elektronentransport im mesoporösen TiO2 kein begrenzender Faktor, da der Transport schneller wird, wenn sich mehr Elektronen ansammeln, was zu einem negativeren Potenzial für EF führt. Mit anderen Worten, der Transportwiderstand Rtr wird kleiner, wenn der TiO2/Elektrolyt-Kondensator CTiO2 aufgeladen ist, siehe Abbildung 2.
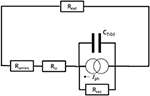
Abbildung 2. Schematisches elektrisches Diagramm einer Farbstoffsolarzelle. Ein Stromgenerator liefert einen Fotostrom Jph, der den Kondensator auflädt. Der Strom fließt durch Rseries + Rtr + Rext und durch Rrec.
Unter Leerlaufbedingungen ist der Außenwiderstand Rext unendlich. Der gesamte Strom fließt dann durch den Rekombinationswiderstand Rrec. Dies ist die normale Bedingung für die Messung der Elektronenlebensdauer τ, die gleich Rrec × CTiO2 ist. Unter Kurzschlussbedingungen ist Rext gleich 0. Der Ladungssammelwirkungsgrad : ηCC ist dann gegeben durch Rrec/(Rseries + Rtr + Rrec), wobei Rseries der unten beschriebene Serienwiderstand ist. Unter MPP-Bedingungen ergibt sich: ηCC = Rrec/(Rseries + Rtr + Rext + Rrec).
Auf der Grundlage dieses einfachen Schemas ist es offensichtlich, dass der Rekombinationswiderstand maximiert werden muss, um die Stromsammel-Effizienz und die Ausgangsspannung über dem externen Widerstand unter MPP-Bedingungen zu erhöhen. Der Rekombinationswiderstand nimmt mit zunehmender Dicke und Oberfläche der mesoporösen Elektrode ab. Mit zunehmender Dicke steigt jedoch der erzeugte Photostrom. Für jedes spezifische DSC-System gibt es eine optimale Schichtdicke: Typische Werte sind ~10 μm für normale Flüssigelektrolyt-DSC und ~2 μm für Festkörper-DSC.
Ein gewisser Serienwiderstandsverlust ist in praktischen DSC-Geräten unvermeidbar. Ein gewisser Widerstand entsteht durch die verwendeten FTO-Substrate, durch den Ladungstransferwiderstand an der Gegenelektrode und durch den Diffusionswiderstand im Elektrolyten. Han et al. führten eine detaillierte Analyse der Widerstände in der DSC durch und minimierten die Rserien auf 1,8 Ohm cm-2, indem sie die katalytische Leistung der Gegenelektrode und den Elektrolytabstand zwischen Arbeits- und Gegenelektrode optimierten (Han et al., 2005). Durch die Minimierung des Abstands zwischen WE und CE wird der Diffusionswiderstand im Elektrolyten minimiert. Es verbleibt jedoch ein Restwiderstand, der durch die Diffusion des Redox-Mediators in den Poren der Arbeitselektrode entsteht. Ein Kurzschluss zwischen WE und CE muss ebenfalls vermieden werden. Die Verwendung von PEDOT auf der Gegenelektrode scheint Kurzschlüsse zu verhindern (Cao et al., 2018).
Komponenten für effizientere DSCs
Mesoporöse Metalloxid-Elektroden
Mesoporöses TiO2 (Anatas) ist die mit Abstand am häufigsten verwendete und bisher erfolgreichste Halbleiterelektrode mit großer Bandlücke, die in DSCs eingesetzt wird. In mehreren Studien wurden die Größe der Nanopartikel, die Porosität des Films und die TiCl4-Nachbehandlung (Ito et al., 2008) optimiert, aber die optimalen Parameter für ein bestimmtes Farbstoffsolarzellensystem hängen stark vom Farbstoff- und Redoxmediatorsystem ab. So eignen sich beispielsweise porösere mesoporöse Filme am besten für DSCs mit Kobaltkomplex als Redox-Mediator. Eine zusätzliche reflektierende TiO2-Schicht wird in der Regel auf eine transparente TiO2-Schicht aufgebracht, um die Lichtausbeute zu verbessern (Ito et al., 2008). Alternativ können auch reflektierende Partikel (Wang et al., 2004) oder Hohlräume (Hore et al., 2005) in den mesoporösen Film eingebaut werden. Eine Oberflächenmodifikation mit ultradünnen Metalloxiden kann von Vorteil sein (Kay und Grätzel, 2002; Kakiage et al., 2015). Dennoch sind einige Eigenschaften von TiO2 nicht ideal: TiO2 ist ein bekannter Photokatalysator. Die Bandlücke von TiO2-Anatas beträgt 3,2 eV, was bedeutet, dass Licht unter 390 nm den Halbleiter anregen kann, was zu hochreaktiven Löchern führt. Die Löcher können zu zerstörerischen Oxidationsreaktionen mit organischen Bestandteilen des DSC führen. UV-Filter werden daher in der Regel für Langzeitstabilitätsstudien von DSC-Bauteilen unter voller Sonneneinstrahlung verwendet. Es gibt Möglichkeiten, die photokatalytische Wirkung von TiO2 zu minimieren, z. B. durch Hinzufügen einer ultradünnen Schicht aus Al2O3 oder MgO (Kay und Grätzel, 2002).
Die Verwendung eines mesoporösen Halbleiters mit einer höheren Bandlücke ist von Vorteil. SnO2 mit einem Eg von 3,6 eV absorbiert nicht so viel UV-Licht aus dem Sonnenspektrum. SnO2 wurde bereits erfolgreich in DSC eingesetzt, aber sein EC liegt im Vergleich zu TiO2 auf einem um etwa 0,5 V positiveren Potenzial, was seine Leistung aufgrund der geringen Ausgangsspannung einschränkt. Durch Bedecken des SnO2 mit einer ultradünnen Metalloxidschicht (wie ZnO, Al2O3 oder MgO) kann eine wesentlich bessere Spannung erzielt werden (Kumara et al., 2001; Kay und Grätzel, 2002).
ZnO wurde intensiv als nanostrukturierte Elektrode in einer Vielzahl von Morphologien in der DSC untersucht (Zhang et al., 2009). Obwohl behauptet wird, dass die besseren Elektronentransporteigenschaften ZnO zu einer besseren nanostrukturierten Elektrode für DSC machen sollten, wurde keine verbesserte Leistung im Vergleich zu den traditionellen mesoporösen TiO2-Elektroden gefunden. Dies liegt daran, dass der Elektronentransport unter Betriebsbedingungen (am MPP) kein limitierender Faktor für die DSC ist. Im Allgemeinen können auch andere Metalloxide als mesoporöse Elektroden in DSC-Geräten fungieren, aber bisher ist ihre Leistung geringer als die ihrer TiO2-Gegenstücke.
Farbstoffe
Wie später erörtert wird, besteht ein Bedarf an dünneren mesoporösen TiO2-Elektroden, der durch neue Redoxvermittler für DSC und Lochleiter für ssDSC entsteht. Daher besteht ein Bedarf an Farbstoffen mit höheren Extinktionskoeffizienten als bei den herkömmlichen Farbstoffen auf der Basis von Ru-Komplexen. Organische Farbstoffe werden daher bevorzugt, wie aus Tabelle 1 mit den besten DSCs hervorgeht. Die Strukturen und einige Absorptionsparameter ausgewählter Farbstoffe sind in Abbildung 3 dargestellt. Viele erfolgreiche organische Farbstoffe haben eine Donor-Pi-Akzeptor (DpA)-Struktur, die bei Photoanregung zu einer Bewegung der Elektronendichte in Richtung des Akzeptorteils führt. Typischerweise ist die Bindungsgruppe in den Akzeptorteil eingebaut, wie im Fall der Cyanoacrylsäure.
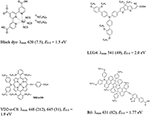
Abbildung 3. Strukturen effizienter molekularer Sensibilisatoren für DSC, mit Absorptionsmaximum (λmax) in nm, Extinktionskoeffizient (in 103 M-1 cm-1) und Null-Null-Übergangsenergie (E0-0). LEG4 ist strukturell fast identisch mit Y123, hat aber Butoxy-Gruppen anstelle von Hexoxy.
Die Farbstoffstruktur spielt eine wichtige Rolle für ihre Gesamtleistung. Ein gutes Blockierverhalten ist entscheidend für den erfolgreichen Einsatz in Kombination mit den neuartigen Redox-Mediatoren oder Lochleitern. Sterische Gruppen können den Elektronentransfer zwischen TiO2 und oxidiertem Redox-Mediator oder Lochleiter verlangsamen (Feldt et al., 2010).
Eine weitere Voraussetzung für eine optimierte Leistung sind Farbstoffe mit relativ langer Lebensdauer im angeregten Zustand und hoher Fluoreszenzausbeute. Schnelle Deaktivierungspfade sollten vermieden werden, da sie die Leistung negativ beeinflussen. Je länger die Anregungslebensdauer ist, desto höher ist die Injektionsleistung. Wang et al. entwickelten eine Reihe von hochfluoreszierenden organischen Farbstoffen mit verbesserten Lebensdauern, wie z. B. R6 mit einer Fluoreszenzlebensdauer von 260 ps für R6, der auf mesoporösem Al2O3-Film adsorbiert ist (Ren et al., 2018).
Die Co-Sensibilisierung ist ein erfolgreicher Weg, um die Leistung der DSC zu verbessern. Rekordgeräte basieren in der Regel auf co-sensibilisierten Solarzellen, siehe Tabelle 1. Eine starke und panchromatische Lichtabsorption kann durch die Auswahl geeigneter Farbstoffe erreicht werden. In mehreren Fällen hat die Ko-Sensibilisierung den positiven Effekt, dass die Farbstoffaggregation verringert wird (Ogura et al., 2009; Hao et al., 2016a). Außerdem kann eine höhere Farbstoffbeladung erzielt werden. Ein interessanter Ansatz ist die Verwendung von Farbstoffen mit unterschiedlichen Bindungsgruppen, die nicht um die gleichen Bindungsstellen auf TiO2 konkurrieren. Shibayama et al. kombinierten erfolgreich den schwarzen Farbstoff (mit Carbonsäure-Bindungsgruppen) mit einem organischen Farbstoff, der eine Pyridin-Bindungsgruppe besitzt (Shibayama et al., 2014). Sie wiesen nach, dass die Farbstoffe an unterschiedlichen Bindungsstellen adsorbieren.
Redox-Mediatoren
Redox-Mediatoren auf Kobaltbasis werden seit 2001 für die DSC getestet (Nusbaumer et al., 2001; Sapp et al., 2002), aber der Durchbruch kam erst 2010 durch die Arbeit von Feldt et al. (2010), die erstmals effiziente DSCs mit Redox-Mediatoren auf Kobaltkomplexbasis durch die Auswahl von Farbstoffen mit geeigneten Eigenschaften demonstrierten. Im Gegensatz zum Triiodid/Iodid-System können Kobaltkomplexe je nach chemischer Struktur ihrer Liganden ein breites Spektrum an Redoxpotentialen aufweisen. Auch die Variation der Gegenionen dieser Komplexe ist wichtig: Dies kann die Löslichkeit in verschiedenen Lösungsmitteln stark beeinflussen. Dies ermöglicht zum Beispiel die Verwendung dieser Redox-Mediatoren in Elektrolyten auf Wasserbasis (Ellis et al., 2016). Interessanterweise wurde über eine gute Stabilität von Elektrolyten berichtet, die auf Wasser basieren (Ellis et al., 2016) oder hohe Konzentrationen von Wasser enthalten (Law et al., 2010), was zu umweltfreundlicheren Solarzellengeräten führen könnte. Die Strukturen und Redoxpotentiale der Kobaltkomplexe sind in Tabelle 1 dargestellt.
Rezente Untersuchungen in unserer Gruppe weisen eindeutig auf ein Problem der derzeitigen Generation von Kobalt-Redox-Mediatoren hin: Sie haben eine relativ langsame Elektronentransferkinetik (Hao et al., 2016b). Die langsame Reduktion von Co3+-Spezies ist vorteilhaft, da sie eine langsame Kinetik für die Elektronenrekombination mit Co3+ ergibt. Andererseits ist die relativ langsame Regeneration der oxidierten Farbstoffmoleküle durch Co2+ ein kritischer Punkt, der die DSC-Leistung einschränkt. Dies wurde in früheren Arbeiten zur kobaltbasierten DSC nicht erkannt. Die Zugabe eines schnellen Elektronendonors, wie z. B. eines Triphenylamins TPA, führt zu einer sehr schnellen Regeneration der oxidierten Farbstoffmoleküle, die auf der Sub-ns-Zeitskala liegt (Hao et al., 2016b). Der oxidierte Donor wird seinerseits durch die Co2+-Spezies reduziert. Infolgedessen wurde ein viel höherer VOC-Wert und ein deutlicher Anstieg der Elektronenlebensdauer festgestellt (siehe Abbildung 4). Die Rekombination zwischen Elektronen in TiO2 und oxidierten Farbstoffmolekülen wird durch das TPA-Additiv stark unterdrückt, was zeigt, dass ohne dieses Additiv eine starke Rekombination stattfand. Infolgedessen stieg die VOC um etwa 100 mV, während das Ladungsextraktionsexperiment zeigte, dass das Bandkantenniveau des TiO2 unverändert war.

Abbildung 4. Wirkung der Zugabe eines TPA-Elektronendonors zum Co(bpy)3-Elektrolyten in einer DSC. (A) Messungen der Ladungsextraktion und (B) der Elektronenlebensdauer als Funktion der VOC in einer DSC mit und ohne Additiv (Hao et al., 2016b).
Interessanterweise führt die Zugabe des Elektronendonors zu einem mittleren Redoxniveau in der DSC. Dies ist der Situation des Triiodid/Iodid-Elektrolyten nicht unähnlich, bei dem das Diiodid-Radikal ein intermediäres Redox-Niveau ergibt (Boschloo und Hagfeldt, 2009).
Eine weitere neuere Entwicklung von Redox-Mediatoren, die weitgehend von unserer Forschungsgruppe vorangetrieben wurde, ist die Verwendung von Kupferkomplexen (Freitag et al., 2015, 2016; Saygili et al., 2016). Diese Mediatoren weisen im Vergleich zu Kobaltkomplexen eine schnellere Farbstoffregenerationskinetik auf (Freitag et al., 2016). Unerwarteterweise wurden relativ lange Elektronenlebensdauern beobachtet. Jüngste Forschungen von Hamann haben gezeigt, dass der Cu2+-Zustand chemisch instabil ist und ein Cu-Komplex mit 4-tert-Butylpyridin gebildet wird, der ein positiveres Potenzial und eine langsame Elektronentransferkinetik aufweist (Wang und Hamann, 2018).
Festkörper-DSCs
Um Festkörper-DSCs herzustellen, kann der flüssige Redox-Elektrolyt durch ein festes Lochtransportmaterial (HTM) ersetzt werden. Die vielversprechendsten Ergebnisse wurden mit molekularen organischen Lochleitern wie Spiro-MeOTAD, leitenden Polymeren wie PEDOT und kürzlich mit Metallkomplexen erzielt (Freitag et al., 2015).
Organische kleinmolekulare HTMs wie Spiro-MeOTAD ermöglichen eine sehr schnelle Farbstoffregeneration im Pikosekundenbereich. Obwohl die Porenfüllung ein Problem darstellen kann, kann bei relativ dünnen mesoporösen TiO2-Filmen in der Regel ein vollständiger Kontakt zwischen Farbstoff und HTM erreicht werden, selbst wenn der Anteil der Porenfüllung weit unter 100 % liegt (Snaith et al., 2008; Cappel et al., 2009; Melas-Kyriazi et al., 2011). Die wichtigsten Einschränkungen der ssDSC ergeben sich aus der sehr schnellen Rekombination zwischen Elektronen in TiO2 und Löchern im HTM (Snaith et al., 2008; Melas-Kyriazi et al., 2011). Dies schränkt die Leistung von ssDSC ein, indem es die Ausgangsspannung deutlich senkt.
Die überraschende Erkenntnis, dass ausgetrocknete DSC mit Cu-Komplex-Redox-Elektrolyt noch als effiziente Solarzellen funktionieren, führte zu einem neuen Typ von ssDSC, der sogenannten Zombie-Solarzelle (Freitag et al., 2015). Jüngste Optimierungen führten zu einem bisherigen Rekordwirkungsgrad von 11,7 % (Zhang et al., 2018). Im Gegensatz zu anderen HTMs werden relativ lange Elektronenlebensdauern gefunden und es können relativ dicke TiO2-Schichten verwendet werden. Die genaue Beschaffenheit des amorphen, getrockneten Elektrolyten HTM, der Cu(tmbpy)2, LiTFSI und vielleicht 4-tert-Butylpyridin enthält, muss noch erforscht werden.
Im Allgemeinen sind ssDSC für die praktische Anwendung sehr attraktiv, aber ihre Leistung muss verbessert werden. Die Einführung eines Redox-Zwischenniveaus könnte hilfreich sein: Es könnte die gebildeten Löcher schnell von der TiO2/Farbstoff-Grenzfläche entfernen.
Abschließende Bemerkungen
Trotz drei Jahrzehnten intensiver Forschung an Farbstoffsolarzellen gibt es noch viele Aspekte zu erforschen, um ihre Leistung weiter zu verbessern. Es gibt nahezu unendlich viele Möglichkeiten, Farbstoffmoleküle zu modifizieren, wobei sterische Gruppen eingeführt werden können, um die Rekombinationsreaktionen zu verlangsamen. Es besteht ein Bedarf an optimalerer Farbstoffpackung auf der TiO2-Oberfläche, um die Lichtabsorption zu erhöhen und einen besseren Blockierungseffekt zu erzielen. Die Co-Sensibilisierung bietet in dieser Hinsicht gute Möglichkeiten. Neuartige Redoxvermittler und HTMs sind der Schlüssel zu einer leistungsfähigeren DSC, da sie eine viel höhere Ausgangsspannung als das herkömmliche Triiodid/Iodid-Redoxpaar bieten können. Leistungsstarke DSC sind für viele Anwendungen interessant, von Stromquellen für die Unterhaltungselektronik bis hin zu gebäudeintegrierten Photovoltaikanlagen und der Stromerzeugung in großem Maßstab. Die Möglichkeit einer hohen Transparenz im nahen Infrarotbereich eröffnet auch die Verwendung von DSC als Top-Zelle in Tandem-Solarzellengeräten.
Autorenbeiträge
Der Autor bestätigt, dass er der einzige Autor dieser Arbeit ist und sie zur Veröffentlichung freigegeben hat.
Erklärung zu Interessenkonflikten
Der Autor erklärt, dass die Forschung in Abwesenheit jeglicher kommerzieller oder finanzieller Beziehungen durchgeführt wurde, die als potenzieller Interessenkonflikt ausgelegt werden könnten.
Danksagungen
STandUP for Energy wird für die Finanzierung gedankt.
Bach, U., Lupo, D., Comte, P., Moser, J. E., Weissortel, F., Salbeck, J., et al. (1998). Farbstoffsensibilisierte mesoporöse TiO2-Solarzellen im Festkörperbetrieb mit hohen Wirkungsgraden bei der Umwandlung von Photonen in Elektronen. Nature 395, 583-585. doi: 10.1038/26936
CrossRef Full Text | Google Scholar
Boschloo, G., and Hagfeldt, A. (2009). Eigenschaften des Jodid/Trijodid-Redox-Mediators in Farbstoffsolarzellen. Acc. Chem. Res. 42, 1819-1826. doi: 10.1021/ar900138m
PubMed Abstract | CrossRef Full Text | Google Scholar
Cao, Y. M., Liu, Y. H., Zakeeruddin, S. M., Hagfeldt, A., and Gratzel, M. (2018). Direkter Kontakt von selektiven Ladungsextraktionsschichten ermöglicht hocheffiziente molekulare Photovoltaik. Joule 2, 1108-1117. doi: 10.1016/j.joule.2018.03.017
CrossRef Full Text | Google Scholar
Cappel, U. B., Gibson, E. A., Hagfeldt, A., and Boschloo, G. (2009). Dye regeneration by spiro-MeOTAD in solid state dye-sensitized solar cells studied by photoinduced absorption spectroscopy and spectroelectrochemistry. J. Phys. Chem. C 113, 6275-6281. doi: 10.1021/jp811196h
CrossRef Full Text | Google Scholar
Ellis, H., Jiang, R., Ye, S., Hagfeld, A., and Boschloo, G. (2016). Entwicklung hocheffizienter Farbstoffsolarzellen mit 100% wässrigem Kobaltelektrolyt. Phys. Chem. Chem. Phys. 18, 8419-8427. doi: 10.1039/C6CP00264A
PubMed Abstract | CrossRef Full Text | Google Scholar
Feldt, S. M.Gibson, E. A., Gabrielsson, E., Sun, L., Boschloo, G., and Hagfeldt, A. (2010). Design von organischen Farbstoffen und Kobalt-Polypyridin-Redox-Mediatoren für hocheffiziente Farbstoffsolarzellen. J. Am. Chem. Soc. 132, 16714-16724. doi: 10.1021/ja1088869
PubMed Abstract | CrossRef Full Text | Google Scholar
Freitag, M., Daniel, Q., Pazoki, M., Sveinbjornsson, K., Zhang, J. B., Sun, L. C., et al. (2015). Hocheffiziente Farbstoffsolarzellen mit molekularem Kupfer-Phenanthrolin als Festkörper-Lochleiter. Energy Environ. Sci. 8, 2634-2637. doi: 10.1039/C5EE01204J
CrossRef Full Text | Google Scholar
Freitag, M., Giordano, F., Yang, W. X., Pazoki, M., Hao, Y., Zietz, B., et al. (2016). Kupfer-Phenanthrolin als schneller und leistungsstarker Redox-Mediator für Farbstoffsolarzellen. J. Phys. Chem. C 120, 9595-9603. doi: 10.1021/acs.jpcc.6b01658
CrossRef Full Text | Google Scholar
Green, M. A. (2012). Grenzwerte für den photovoltaischen Wirkungsgrad unter neuen, auf ASTM International G173 basierenden Referenzspektren. Prog. Photovoltaics 20, 954-959. doi: 10.1002/pip.1156
CrossRef Full Text | Google Scholar
Hagfeldt, A., Boschloo, G., Sun, L., Kloo, L., and Pettersson, H. (2010). Dye-sensitized solar cells. Chem. Rev. 110, 6595-6663. doi: 10.1021/cr900356p
CrossRef Full Text | Google Scholar
Han, L. Y., Islam, A., Chen, H., Malapaka, C., Chiranjeevi, B., Zhang, S. F., et al. (2012). Hocheffiziente Farbstoffsolarzelle mit einem neuartigen Co-Adsorbens. Energy Environ. Sci. 5, 6057-6060. doi: 10.1039/c2ee03418b
CrossRef Full Text | Google Scholar
Han, L. Y., Koide, N., Chiba, Y., Islam, A., Komiya, R., Fuke, N., et al. (2005). Verbesserung der Effizienz von Farbstoffsolarzellen durch Verringerung des Innenwiderstands. Appl. Phys. Lett. 86:213501. doi: 10.1063/1.1925773
CrossRef Full Text | Google Scholar
Hao, Y., Saygili, Y., Cong, J. Y., Eriksson, A., Yang, W. X., Zhang, J. B., et al. (2016a). Novel blue organic dye for dye-sensitized solar cells achieving high efficiency in cobalt-based electrolytes and by co-sensitization. Acs Appl. Mater. Interfaces 8, 32797-32804. doi: 10.1021/acsami.6b09671
PubMed Abstract | CrossRef Full Text | Google Scholar
Hao, Y., Yang, W. X., Zhang, L., Jiang, R., Mijangos, E., Saygili, Y., et al. (2016b). Ein kleiner Elektronendonor im Kobaltkomplex-Elektrolyt verbessert die Effizienz von Farbstoffsolarzellen erheblich. Nat. Commun. 7:13934. doi: 10.1038/ncomms13934
PubMed Abstract | CrossRef Full Text | Google Scholar
Haque, S. A., Palomares, E., Cho, B. M., Green, A. N. M., Hirata, N., Klug, D. R., et al. (2005). Charge separation versus recombination in dye-sensitized nanocrystalline solar cells: the minimization of kinetic redundancy. J. Am. Chem. Soc. 127, 3456-3462. doi: 10.1021/ja0460357
PubMed Abstract | CrossRef Full Text | Google Scholar
Haque, S. A., Tachibana, Y., Willis, R. L., Moser, J. E., Grätzel, M., David, R., et al. (2000). Parameter, die die Kinetik der Ladungsrekombination in farbstoffsensibilisierten nanokristallinen Titandioxidfilmen beeinflussen. J. Phys. Chem. B 104, 538-547. doi: 10.1021/jp991085x
CrossRef Full Text | Google Scholar
Hore, S., Nitz, P., Vetter, C., Prahl, C., Niggemann, M., and Kern, R. (2005). Streuende sphärische Hohlräume in nanokristallinem TiO2 – Steigerung der Effizienz in Farbstoffsolarzellen. Chem. Commun. 15, 2011-2013. doi: 10.1039/b418658n
CrossRef Full Text | Google Scholar
Ito, S., Murakami, T. N., Comte, P., Liska, P., Gratzel, C., Nazeeruddin, M. K., et al. (2008). Herstellung von farbstoffsensibilisierten Dünnschichtsolarzellen mit einem Wirkungsgrad von über 10 % bei der Umwandlung von Sonnenenergie in elektrische Energie. Thin Solid Films 516, 4613-4619. doi: 10.1016/j.tsf.2007.05.090
CrossRef Full Text | Google Scholar
Kakiage, K., Aoyama, Y., Yano, T., Oya, K., Fujisawa, J., and Hanaya, M. (2015). Highly-efficient dye-sensitized solar cells with collaborative sensitization by silyl-anchor and carboxy-anchor dyes. Chem. Commun. 51, 15894-15897. doi: 10.1039/C5CC06759F
PubMed Abstract | Querverweis Volltext | Google Scholar
Kakiage, K., Osada, H., Aoyama, Y., Yano, T., Oya, K., Iwamoto, S., et al. (2016). Achievement of over 1.4 V photovoltage in a dye-sensitized solar cell by the application of a silyl-anchor coumarin dye. Sci. Rep. 6:35888. doi: 10.1038/srep35888
PubMed Abstract | CrossRef Full Text | Google Scholar
Kay, A., and Grätzel, M. (2002). Dye-sensitized core-shell nanocrystals: improved efficiency of mesoporous tin oxide electrodes coated with a thin layer of an insulating oxide. Chem. Mater. 14, 2930-2935. doi: 10.1021/cm0115968
CrossRef Full Text | Google Scholar
Kumara, G., Tennakone, K., Perera, V. P. S., Konno, A., Kaneko, S., and Okuya, M. (2001). Unterdrückung von Rekombinationen in einer farbstoffsensibilisierten photoelektrochemischen Zelle aus einem Film aus Zinn-IV-Oxidkristalliten, der mit einer dünnen Schicht Aluminiumoxid beschichtet ist. J. Phys. D-Appl. Phys. 34, 868-873. doi: 10.1088/0022-3727/34/6/306
CrossRef Full Text | Google Scholar
Law, C., Pathirana, S. C., Li, X., Anderson, A. Y., Barnes, P. R. F., Listorti, A., et al. (2010). Wasserbasierte Elektrolyte für farbstoffsensibilisierte Solarzellen. Adv. Mater. 22, 4505-4509. doi: 10.1002/adma.201001703
PubMed Abstract | CrossRef Full Text | Google Scholar
Mathew, S., Yella, A., Gao, P., Humphry-Baker, R., Curchod, B. F. E., Ashari-Astani, N., et al. (2014). Farbstoffsensibilisierte Solarzellen mit einem Wirkungsgrad von 13 % durch molekulares Engineering von Porphyrin-Sensibilisatoren. Nat. Chem. 6, 242-247. doi: 10.1038/nchem.1861
PubMed Abstract | CrossRef Full Text | Google Scholar
Melas-Kyriazi, J., Ding, I. K., Marchioro, A., Punzi, A., Hardin, B. E., Burkhard, G. F., et al. (2011). The effect of hole transport material pore filling on photovoltaic performance in solid-state dye-sensitized solar cells. Adv. Energy Mater. 1, 407-414. doi: 10.1002/aenm.201100046
CrossRef Full Text | Google Scholar
Nusbaumer, H., Moser, J. E., Zakeeruddin, S. M., Nazeeruddin, M. K., and Gratzel, M. (2001). Co-II(dbbiP)(2)(2+) complex rivals tri-iodide/iodide redox mediator in dye-sensitized photovoltaic cells. J. Phys. Chem. B 105, 10461-10464. doi: 10.1021/jp012075a
CrossRef Full Text | Google Scholar
Ogura, R. Y., Nakane, S., Morooka, M., Orihashi, M., Suzuki, Y., and Noda, K. (2009). Hochleistungs-Farbstoffsolarzelle mit einem Mehrfach-Farbstoffsystem. Appl. Phys. Lett. 94:073308. doi: 10.1063/1.3086891
CrossRef Full Text | Google Scholar
O’Regan, B., and Grätzel, M. (1991). Eine kostengünstige, hocheffiziente Solarzelle auf der Basis von farbstoffsensibilisierten kolloidalen Titandioxidfilmen. Nature 353, 737-740. doi: 10.1038/353737a0
CrossRef Full Text | Google Scholar
Ren, Y. M., Sun, D. Y., Cao, Y. M., Tsao, H. N., Yuan, Y., Zakeeruddin, S. M., et al. (2018). Ein stabiler blauer Photosensibilisator für die Farbpalette von Farbstoffsolarzellen mit einem Wirkungsgrad von 12,6 %. J. Am. Chem. Soc. 140, 2405-2408. doi: 10.1021/jacs.7b12348
PubMed Abstract | CrossRef Full Text | Google Scholar
Sapp, S. A., Elliott, C. M., Contado, C., Caramori, S., and Bignozzi, C. A. (2002). Substituierte Polypyridin-Komplexe von Kobalt(II/III) als effiziente Elektronenübertragungsmediatoren in Farbstoffsolarzellen. J. Am. Chem. Soc. 124, 11215-11222. doi: 10.1021/ja027355y
PubMed Abstract | CrossRef Full Text | Google Scholar
Saygili, Y., Soderberg, M., Pellet, N., Giordano, F., Cao, Y. M., Munoz-Garcia, A. B., et al. (2016). Kupfer-Bipyridyl-Redox-Mediatoren für farbstoffsensibilisierte Solarzellen mit hoher Photospannung. J. Am. Chem Soc. 138, 15087-15096. doi: 10.1021/jacs.6b10721
PubMed Abstract | CrossRef Full Text | Google Scholar
Shen, Z. J., Xu, B., Liu, P., Hu, Y., Yu, Y., Ding, H. R., et al. (2017). Hochleistungsfähige Festkörper-Farbstoffsolarzellen auf Basis organischer blauer Farbstoffe. J. Mater. Chem. A 5, 1242-1247. doi: 10.1039/C6TA09723E
CrossRef Full Text | Google Scholar
Shibayama, N., Ozawa, H., Abe, M., Ooyama, Y., and Arakawa, H. (2014). A new cosensitization method using the Lewis acid sites of a TiO2 photoelectrode for dye-sensitized solar cells. Chem. Commun. 50, 6398-6401. doi: 10.1039/C3CC49461F
CrossRef Full Text | Google Scholar
Snaith, H. J., Humphry-Baker, R., Chen, P., Cesar, I., Zakeeruddin, S. M., and Grätzel, M. (2008). Ladungssammlung und Porenfüllung in Farbstoffsolarzellen in festem Zustand. Nanotechnology 19:424003. doi: 10.1088/0957-4484/19/42/424003
PubMed Abstract | CrossRef Full Text | Google Scholar
Wang, Y., and Hamann, T. W. (2018). Verbesserte Leistung durch in situ Ligandenaustauschreaktionen von Kupfer-Bipyridyl-Redoxpaaren in Farbstoffsolarzellen. Chem. Commun. 54, 12361-12364. doi: 10.1039/C8CC07191H
PubMed Abstract | CrossRef Full Text | Google Scholar
Wang, Z. S., Kawauchi, H., Kashima, T., and Arakawa, H. (2004). Signifikanter Einfluss der Morphologie der TiO2-Photoelektrode auf die Energieumwandlungseffizienz der Farbstoffsolarzelle N719. Coord. Chem. Rev. 248, 1381-1389. doi: 10.1016/j.ccr.2004.03.006
CrossRef Full Text | Google Scholar
Yella, A., Lee, H. W., Tsao, H. N., Yi, C., Chandiran, A. K., Nazeeruddin, M. K., et al. (2011). Porphyrin-sensibilisierte Solarzellen mit Redox-Elektrolyten auf Kobalt(II/III)-Basis übertreffen 12 Prozent Wirkungsgrad. Science 334, 629-634. doi: 10.1126/science.1209688
PubMed Abstract | CrossRef Full Text | Google Scholar
Yum, J. H., Baranoff, E., Kessler, F., Moehl, T., Ahmad, S., Bessho, T., et al. (2012). Ein Kobaltkomplex-Redox-Shuttle für Farbstoffsolarzellen mit hohen Leerlaufpotentialen. Nat. Commun. 3:631. doi: 10.1038/ncomms1655
PubMed Abstract | CrossRef Full Text | Google Scholar
Zhang, Q. F., Dandeneau, C. S., Zhou, X. Y., and Cao, G. Z. (2009). ZnO-Nanostrukturen für farbstoffsensibilisierte Solarzellen. Adv. Mater. 21, 4087-4108. doi: 10.1002/adma.200803827
CrossRef Full Text | Google Scholar
Zhang, W., Wu, Y., Bahng, H. W., Cao, Y., Yi, C., Saygili, Y., et al. (2018). Umfassende Kontrolle des Spannungsverlustes ermöglicht 11,7 % effiziente Festkörper-Farbstoffsolarzellen. Energy Environ. Sci. 11, 1779-1787. doi: 10.1039/C8EE00661J
CrossRef Full Text | Google Scholar