INTRODUCCIÓN
La endocarditis infecciosa (EI) del lado derecho es frecuente en los drogadictos por vía intravenosa y representa el 35%-60% de los casos de endocarditis en esta población.1,2 Antes del aumento de la adicción a las drogas por vía intravenosa en las últimas décadas, la endocarditis derecha era rara y se producía casi exclusivamente en pacientes con malformaciones cardíacas.3,4 Según las estimaciones actuales de grandes series, sólo el 5%-10% de las EI derechas aparecen en pacientes no adictos.5,6 Los diagnósticos definitivos de EI derecha son excepcionales en pacientes no adictos sin cardiopatía predisponente. Se han descrito muy pocos casos de este tipo en la literatura y su diagnóstico puede suponer un importante reto clínico.7
Describimos el caso de un hombre sin antecedentes de venopunción, diagnosticado recientemente en nuestro servicio de endocarditis de la válvula tricúspide en una válvula morfológicamente normal.
CASO CLÍNICO
Un hombre de 57 años de edad, con antecedentes sólo destacables por una úlcera duodenal inactiva desde hacía varios años, fue ingresado por un síndrome febril (hasta 40°C) de siete días de duración, fuertes dolores articulares y musculares generalizados con importante postración, lesiones cutáneas rojizas puntiformes en ambas piernas e inflamación del hombro y codo izquierdos. No presentaba ningún foco clínico infeccioso del tracto respiratorio, abdominal, genitourinario u otorrinolaringológico. Negó el uso de drogas inyectables o catéteres intravenosos. No tenía hábito de consumo de alcohol, ni conductas de riesgo para enfermedades de transmisión sexual, ni procedimientos dentales recientes. No tenía antecedentes de fiebre reumática. La historia clínica del paciente incluía una pequeña lesión superficial en el codo izquierdo que se había producido 5 semanas antes y que tardó varios días en curar.
La exploración física mostraba una temperatura de 38°C, crepitaciones finas en el tercio inferior de ambos campos pulmonares, una importante limitación de la movilidad por intensos dolores articulares y musculares, signos de inflamación en las articulaciones acromioclaviculares y esternoclaviculares izquierdas y, en menor grado, en el codo izquierdo, y múltiples lesiones purpúricas-petecales en ambas piernas, que eran negativas en la diascopia. Todos los demás aspectos de la exploración física completa eran normales. No había estigmas cutáneos o mucosos de endocarditis, marcas de venopunción, soplos cardíacos, linfadenopatías, signos de meningismo o síntomas neurológicos.
Los análisis de laboratorio revelaron anemia normocítica (10.5 g/dL de hemoglobina), leucocitosis (23 000/μL) con neutrofilia (85%), alteraciones del panel hepático con colestasis moderada (bilirrubina, 2,0 mg/dL; fosfatasa alcalina, 416 U/L; GGT, 75 U/L), y hematuria microscópica (20 RBCs por campo). En la radiografía de tórax se observaba una afectación del parénquima basal bilateral. La serología para el virus de la inmunodeficiencia humana fue negativa. El Staphylococcus aureus sensible a la oxacilina creció en los cuatro hemocultivos y la ecocardiografía transesofágica mostró una vegetación filiforme móvil, de 16×3 mm, en la valva lateral de la válvula tricúspide, que era morfológicamente normal aparte de esta característica (Figura 1). No había signos de vegetaciones en las válvulas mitral, aórtica o pulmonar, que eran todas normales. Estos hallazgos fueron corroborados en el estudio transesofágico de seguimiento realizado 24 días después.
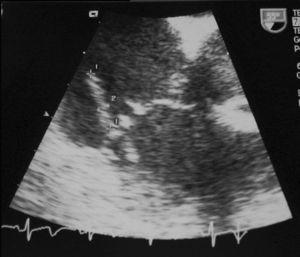
Fig. 1. Ecocardiograma transesofágico que muestra una imagen filiforme móvil, de 16×3 mm, insertada en el segmento medial de la vertiente auricular de la valva lateral de la válvula tricúspide, consistente con una vegetación.
La tomografía computarizada (TC) de tórax (figura 2) mostró múltiples nódulos pulmonares periféricos, sugerentes de émbolos sépticos. No se observaron alteraciones en las radiografías de hombros y codos. Se estableció el diagnóstico de EI de la válvula tricúspide nativa sin una condición predisponente clara. No se identificó con precisión el portal de entrada, aunque se consideró la lesión cutánea del codo izquierdo descrita por la paciente, aunque no había evidencia significativa de inflamación. La endocarditis se complicó con afectación pulmonar asintomática, anemia, púrpura vasculítica y oligoartritis, probablemente debido a un mecanismo inmunológico. No se realizó biopsia de piel ya que las lesiones estaban remitiendo, y no se estudió el líquido sinovial por su escasa cantidad.

Fig. 2. Imagen de tomografía computarizada de tórax que muestra varios nódulos pequeños, bilaterales, periféricos y subpleurales, con cavitación en algunos casos, que sugieren émbolos sépticos. Las opacidades en forma de cuña con broncograma aéreo interno, en el que la base está en contacto con la pleura, sugieren pequeños infartos pulmonares.
Se inició tratamiento con cloxacilina parenteral a dosis de 2 g/4 h. Este tratamiento se cambió por cefazolina tras observarse hallazgos compatibles con nefritis intersticial inmunoalérgica (deterioro de la función renal con importante eosinofilia periférica y eosinofiluria, todo ello resuelto con el cambio de antibiótico), aunque no hubo confirmación histológica. El estudio de provocación posterior no se consideró apropiado. Tras 6 semanas de tratamiento antibiótico intravenoso específico, los hemocultivos fueron negativos, el paciente estaba hemodinámicamente estable y los síntomas articulares se habían resuelto por completo, sin dejar secuelas radiológicas.
DISCUSIÓN
La endocarditis infecciosa es infrecuente en pacientes que no son drogadictos y no tienen ninguna cardiopatía predisponente.8 La infección de las válvulas cardíacas derechas aparece en el 5%-10% de todos los casos de endocarditis infecciosa1,5,6,9,10 y se asocia casi siempre con el abuso de drogas intravenosas, que es, con mucho, el factor predisponente más común, ya que más del 80% de los casos de endocarditis de la válvula tricúspide se dan en drogadictos.11 La EI del lado derecho se produce con mucha menos frecuencia en pacientes no adictos como complicación de la colocación de catéteres intravenosos permanentes, infecciones cutáneas o genitales no tratadas,10,12,13 o cardiopatías congénitas subyacentes.4 La afectación de la válvula tricúspide en un paciente sin condiciones predisponentes y con un corazón estructuralmente normal, como ocurrió en el paciente descrito, es una rareza clínica en la que el diagnóstico puede ser bastante complicado.7 No hay grandes estudios que hayan considerado y cuantificado la frecuencia y las características clínicas de esta afección.
En general, la EI aislada de la válvula tricúspide nativa en adultos no adictos se produce en pacientes jóvenes, hasta la quinta década de la vida.8,14 En la mayoría de los casos (70%), existen condiciones médicas subyacentes (alcoholismo, aborto, enfermedad de colon, inmunodeficiencia, catéteres permanentes, proceso séptico en la cavidad oral, la piel o los genitales, etc.).7,10,12,14 Ninguna de estas condiciones fue claramente identificada en el caso presentado.
Desde el punto de vista etiológico, el patógeno más frecuentemente aislado es S aureus (aunque en un porcentaje menor al descrito en drogadictos). El portal de entrada del microorganismo en el torrente sanguíneo no siempre está determinado, como parecía ocurrir en el presente caso, en el que la lesión cutánea no era concluyente. Nunca se identificó un proceso inflamatorio de la piel que pudiera haber sido el foco bacteriémico de la infección. No obstante, la bacteriemia suele ser endógena y adquirida en la comunidad, y la piel es el portal de entrada más común, sobre todo en el caso de S aureus.7,8,14 Otras fuentes de infección son el tracto genitourinario y el colon.13,14
La presentación clínica consiste invariablemente en fiebre persistente asociada a eventos pulmonares (generalmente asintomáticos), anemia y hematuria microscópica, signos que constituyen el «síndrome tricuspídeo», según la descripción de Nandakumar y Raju.7 Cabe destacar la ausencia de estigmas periféricos de endocarditis o soplos relevantes en la mayoría de los casos. El soplo de regurgitación tricuspídea no suele detectarse en el momento en que se presentan los signos y síntomas, como ocurrió en el caso descrito. Entre las manifestaciones sistémicas, los signos articulares, musculares y cutáneos que predominan en el cuadro presentado por nuestra paciente no están incluidos en los datos clínicos típicos descritos para pacientes no adictos con EI de la válvula tricúspide nativa en las principales series.7,12,14 Este hecho hace aún más inusual el caso descrito, en el que se descartó la afectación del corazón izquierdo mediante 2 ecocardiogramas transesofágicos en un intervalo de más de 3 semanas.
Como en cualquier caso de EI, el cuadro clínico, los hallazgos positivos en los hemocultivos y la ecocardiografía (el gold standard) son las principales herramientas diagnósticas en la EI de válvula tricúspide nativa. En general, el pronóstico es excelente con el tratamiento médico (la terapia antibiótica específica y el apoyo tienen una alta tasa de éxito) y el desarrollo de la insuficiencia cardíaca es infrecuente. Sólo el 25% de los casos requieren una sustitución valvular o una intervención quirúrgica. Las indicaciones para esta última opción son las mismas que en cualquier paciente con EI: fracaso del tratamiento antibiótico con fiebre persistente o insuficiencia cardíaca derecha.4,10,15 La mortalidad asociada a la EI de la válvula tricúspide nativa es menor que la descrita para la endocarditis en pacientes con una condición predisponente.8
.