INTRODUCTION
L’endocardite infectieuse (EI) droite est fréquente chez les toxicomanes par voie intraveineuse et représente 35 à 60 % des cas d’endocardite dans cette population1,2. Avant l’augmentation de la toxicomanie par voie intraveineuse au cours des dernières décennies, l’endocardite du côté droit était rare et survenait presque exclusivement chez des patients présentant des malformations cardiaques.3,4 Selon les estimations actuelles issues de grandes séries, seuls 5 % à 10 % des EI du côté droit apparaissent chez des patients non toxicomanes.5,6 Les diagnostics définitifs d’EI du côté droit sont exceptionnels chez les patients non toxicomanes sans cardiopathie prédisposante. Très peu de cas de ce type ont été rapportés dans la littérature et leur diagnostic peut représenter un défi clinique important7.
Nous décrivons le cas d’un homme sans antécédent de ponction veineuse, récemment diagnostiqué dans notre service avec une endocardite de la valve tricuspide dans une valve morphologiquement normale.
ÉTUDE DE CAS CLINIQUE
Un homme de 57 ans, aux antécédents remarquables uniquement pour un ulcère duodénal inactif depuis plusieurs années, a été admis pour un syndrome fébrile (jusqu’à 40°C) de sept jours, des douleurs articulaires et musculaires sévères généralisées avec une prostration importante, des lésions cutanées en forme de points rougeâtres sur les deux jambes et une inflammation de l’épaule et du coude gauche. Il ne présentait aucun foyer infectieux clinique des voies respiratoires, abdominales, génito-urinaires ou oto-rhino-laryngologiques. Il a nié l’utilisation de drogues injectables ou de cathéters intraveineux. Il n’avait pas d’habitude d’alcool, de comportement à risque pour les maladies sexuellement transmissibles ou de procédures dentaires récentes. Il n’avait pas d’antécédents de rhumatisme articulaire aigu. Les antécédents cliniques des patients comprenaient une petite lésion superficielle sur le coude gauche qui était survenue 5 semaines auparavant et qui avait mis plusieurs jours à guérir.
L’examen physique a montré une température de 38°C, des crépitants fins en fin d’inspiration dans le tiers inférieur des deux champs pulmonaires, une limitation importante de la mobilité en raison de douleurs articulaires et musculaires intenses, des signes d’inflammation dans les articulations acromioclaviculaire et sternoclaviculaire gauches et, à un moindre degré, dans le coude gauche, et de multiples lésions purpuriques-pétéchiales en forme de points sur les deux jambes, qui étaient négatives à la diascopie. Tous les autres aspects de l’examen physique complet étaient normaux. Il n’y avait pas de stigmates cutanés ou muqueux d’endocardite, de marques de ponction veineuse, de souffle cardiaque, de lymphadénopathie, de signes de méningisme ou de symptômes neurologiques.
Les analyses de laboratoire ont révélé une anémie normocytaire (10.5 g/dL d’hémoglobine), une leucocytose (23 000/μL) avec neutrophilie (85 %), des altérations du bilan hépatique avec cholestase modérée (bilirubine, 2,0 mg/dL ; phosphatase alcaline, 416 U/L ; GGT, 75 U/L) et une hématurie microscopique (20 GR par champ). Une atteinte bilatérale du parenchyme basal a été constatée à la radiographie pulmonaire. La sérologie du virus de l’immunodéficience humaine était négative. Le Staphylococcus aureus sensible à l’oxacilline s’est développé dans les quatre hémocultures et l’échocardiographie transoesophagienne a montré une végétation filiforme mobile de 16×3 mm dans le feuillet latéral de la valve tricuspide, qui était morphologiquement normale à part cette caractéristique (Figure 1). Il n’y avait aucun signe de végétations dans les valves mitrale, aortique ou pulmonaire, qui étaient toutes normales. Ces résultats ont été corroborés dans l’étude transœsophagienne de suivi effectuée 24 jours plus tard.
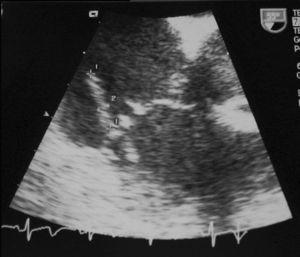
Fig. 1. Echocardiographie transoesophagienne montrant une image filiforme mobile de 16×3 mm insérée dans le segment médian de la face auriculaire du feuillet latéral de la valve tricuspide, compatible avec une végétation.
La tomodensitométrie (TDM) thoracique (figure 2) a montré de multiples nodules pulmonaires périphériques, suggérant des emboles septiques. Aucune altération n’a été observée sur les radiographies des épaules et des coudes. Le diagnostic d’EI de la valve tricuspide native sans condition prédisposante claire a été établi. La porte d’entrée n’a pas été identifiée précisément, bien que la lésion cutanée du coude gauche décrite par le patient ait été envisagée, même s’il n’y avait pas de preuve significative d’inflammation. L’endocardite s’est compliquée d’une atteinte pulmonaire asymptomatique, d’une anémie, d’un purpura vasculaire et d’une oligoarthrite, probablement dus à un mécanisme immunologique. Une biopsie cutanée n’a pas été réalisée car les lésions régressaient, et le liquide synovial n’a pas été étudié en raison de sa faible quantité.

Fig. 2. Image de tomodensitométrie thoracique montrant divers petits nodules bilatéraux, périphériques et sous-pleuraux, avec cavitation dans certains cas, suggérant des emboles septiques. Les opacités cunéiformes avec un bronchogramme à air interne, dont la base est en contact avec la plèvre, suggèrent de petits infarctus pulmonaires.
Un traitement par cloxacilline parentérale à la dose de 2 g/4 h a été débuté. Ce traitement a été remplacé par de la céfazoline après que des résultats compatibles avec une néphrite interstitielle immunoallergique aient été observés (détérioration de la fonction rénale avec une éosinophilie périphérique significative et une éosinophilurie, qui ont toutes disparu avec le changement d’antibiotique), bien qu’il n’y ait pas eu de confirmation histologique. Une étude de provocation ultérieure n’a pas été jugée appropriée. Après 6 semaines d’antibiothérapie intraveineuse spécifique, les hémocultures étaient négatives, le patient était stable sur le plan hémodynamique et les symptômes articulaires avaient complètement disparu, ne laissant aucune séquelle radiologique.
DISCUSSION
L’endocardite infectieuse est rare chez les patients qui ne sont pas toxicomanes et ne présentent pas de cardiopathie prédisposante8. L’infection des valves cardiaques droites apparaît dans 5 % à 10 % de tous les cas d’endocardite infectieuse1,5,6,9,10 et est presque toujours associée à l’abus de drogues par voie intraveineuse, de loin le facteur de prédisposition le plus fréquent, plus de 80 % des cas d’endocardite de la valve tricuspide survenant chez des toxicomanes.11 L’EI droite est beaucoup moins fréquente chez les patients non toxicomanes, comme complication de la pose d’un cathéter intraveineux permanent, d’infections cutanées ou génitales non traitées10,12,13 ou d’une cardiopathie congénitale sous-jacente.4 L’atteinte de la valve tricuspide chez un patient ne présentant aucune condition prédisposante et dont le cœur est structurellement normal, comme c’est le cas du patient décrit, est une rareté clinique dont le diagnostic peut être assez compliqué.7 Aucune étude d’envergure n’a examiné et quantifié la fréquence et les caractéristiques cliniques de cette affection.
Généralement, l’EI isolée de la valve tricuspide native chez les adultes non toxicomanes survient chez des patients plus jeunes, jusqu’à la cinquième décennie de vie.8,14 Dans la majorité des cas (70%), il existe des conditions médicales sous-jacentes (alcoolisme, avortement, maladie du côlon, immunodéficience, cathéters permanents, processus septique dans la cavité orale, la peau ou les organes génitaux, etc.).7,10,12,14 Aucune de ces conditions n’a été clairement identifiée dans le cas présenté.
Du point de vue étiologique, l’agent pathogène le plus souvent isolé est S aureus (bien que dans un pourcentage plus faible que celui qui a été décrit chez les toxicomanes). La porte d’entrée du micro-organisme dans la circulation sanguine n’est pas toujours déterminée, comme cela semblait être le cas dans le présent dossier, où la lésion cutanée n’était pas probante. Un processus cutané inflammatoire qui aurait pu être le foyer bactérien de l’infection n’a jamais été identifié. Néanmoins, la bactériémie est généralement endogène et communautaire, et la peau est la porte d’entrée la plus courante, en particulier dans le cas de S aureus.7,8,14 Les autres sources d’infection sont les voies génito-urinaires et le côlon13,14.
La présentation clinique consiste invariablement en une fièvre persistante associée à des manifestations pulmonaires (généralement asymptomatiques), une anémie et une hématurie microscopique, signes qui constituent le » syndrome tricuspidien « , selon la description de Nandakumar et Raju.7 Il convient de noter l’absence de stigmates périphériques d’endocardite ou de souffle pertinent dans la majorité des cas. Le souffle de la régurgitation tricuspide n’est généralement pas détecté au moment où les signes et les symptômes se manifestent, comme cela s’est produit dans le cas décrit. Parmi les manifestations systémiques, les signes articulaires, musculaires et cutanés qui dominent dans le tableau présenté par notre patient ne sont pas inclus dans les données cliniques typiques décrites pour les patients non dépendants avec une EI de la valve tricuspide native dans les principales séries.7,12,14 Ce fait rend le cas décrit, dans lequel une atteinte du cœur gauche a été exclue par deux échocardiogrammes transœsophagiens dans un intervalle de plus de 3 semaines, encore plus inhabituel.
Comme dans tout cas d’EI, le tableau clinique, les résultats positifs des hémocultures et l’échocardiographie (l’étalon-or) sont les principaux outils diagnostiques de l’EI de la valve tricuspide native. En général, le pronostic est excellent avec un traitement médical (une antibiothérapie spécifique et un soutien ont un taux de réussite élevé) et le développement d’une insuffisance cardiaque est rare. Seuls 25 % des cas nécessitent un remplacement de la valve ou une intervention chirurgicale. Les indications pour cette dernière option sont les mêmes que pour tout patient atteint d’EI : échec de l’antibiothérapie avec fièvre persistante ou insuffisance cardiaque droite.4,10,15 La mortalité associée à l’EI de la valve tricuspide native est inférieure à celle décrite pour l’endocardite chez les patients présentant une condition prédisposante.8