MAGYARORSZÁGON A SZEMBENNYILVÁNTARTALMAS NYOMÁSLEVEGYELEM csökkentésére használt gyógyszerek többsége szemcsepp formájában áll rendelkezésre. Ennek a tendenciának megfelelően, amikor szénsav anhidráz gátlókat írnak fel, azok általában helyileg alkalmazandók. A Diamoxhoz (acetazolamid) és a Neptazane-hoz (metazolamid) hasonló szájon át szedhető CAI-któl való elmozdulást az olyan hatásos helyi gyógyszercsoportok, mint a prosztaglandin analógok és az alfa-agonisták kifejlesztése is felgyorsította.
Valójában egyre könnyebben figyelmen kívül lehet hagyni az orális CAI-kat, amikor arról döntünk, hogyan kezeljük a beteget. Pedig nagyon hatékony munkát végezhetnek az IOP csökkentésében és biztonságos szinten tartásában. Itt szeretnék emlékeztetni néhány olyan helyzetre, amelyben ezek a gyógyszerek hasznosak lehetnek.
Egy hatékony lehetőség
Az elsődleges ok, amiért az orális CAI-kat nem írják fel olyan gyakran, mint a helyi cseppeket, a szisztémás mellékhatások lehetősége, amelyek a szemcseppeknél ritkák. A Diamox, különösen nagyobb dózisban, sok betegnél bizsergést, gyomor-bélrendszeri zavarokat és fokozott vizeletürítést okoz, és egyéb súlyosabb problémák is lehetségesek. A Neptazane-nak kevesebb mellékhatása van, mint a Diamoxnak, de ez egy gyengébb gyógyszer is.
A metazolamid és az acetazolamid hatékonyan csökkenti az IOP-t, és olyan módon alkalmazható, hogy minimalizálja vagy megszünteti a lehetséges mellékhatásokat.
A tény azonban továbbra is az, hogy az orális CAI-k hatékonyak. A Diamox napközben 21-30 százalékkal, éjszaka pedig 24 százalékkal csökkenti a vízelfolyást (ez az előny a béta-blokkolókkal nem azonos).1,2 És sok betegnél tapasztaltam, hogy az orális CAI-k jelentősen hatékonyabbak, mint a lokális CAI-k. Voltak dorzolamidot használó betegeim, akiket 40 mmHg-os IOP-val küldtek hozzám; Diamoxot adtam nekik, és a nyomásuk 25 mmHg-ra csökkent. Egy tanulmány szerint a Diamox hozzáadása a dorzolamidhoz további 16 százalékkal csökkentette az IOP-t, míg a dorzolamid hozzáadása a Diamoxhoz nem volt hatásos.1
Nem minden szakirodalom ért egyet az orális és a lokális CAI-k összehasonlító értékét illetően; egyes tanulmányok3-5 szerint az orális gyógyszerek hatékonyabbak, mint a lokálisak, míg mások alig találtak különbséget.6-8 Klinikai tapasztalataim azonban nem hagytak kétséget afelől, hogy az orális CAI-k sok egyénnél hatékonyabbak lehetnek.
A mellékhatások lehetősége miatt ezeket a gyógyszereket néha olyan helyzetekre tartják fenn, amikor a beteg glaukómája súlyos. A szokásos gyakorlatban a legtöbb beteg nem tartozna ebbe a kategóriába – ami megmagyarázhatja, hogy egyes orvosok miért feledkeznek meg erről a lehetőségről. Olyan beutalóhelyzetben vagyok, ahol az emberek folyamatosan küldenek nekem olyan betegeket, akik nagyon rossz állapotban vannak. Ennek eredményeképpen gyakran folyamodom ehhez a lehetőséghez.
Mikor segíthetnek az orális CAI-k
Az orális CAI-k alkalmazásának elsősorban akkor van értelme, ha a mellékhatásokat más megfontolások enyhítik vagy ellensúlyozzák. Íme néhány olyan körülmény, amikor kiváló eredménnyel írtam fel orális CAI-kat:
– Az IOP ideiglenes alacsonyan tartása. Az orális CAI kiváló módja lehet az időnyerésnek, ha a helyi gyógyszereket már alkalmazó betegnél nem tudnak időpontot szabni a glaukómashunt vagy más eszköz beültetésére szolgáló műtétre. Mivel a gyógyszer alkalmazása nagyon rövid ideig tart, a mellékhatásoknak általában nincs ideje kialakulni.
Az egyik akut neovaszkuláris glaukómás betegem például részleges panretinalis fotokoaguláción esett át, de még mindig 48 mmHg volt az IOP-je. További PRP volt egy járható út, és úgy éreztem, hogy ez előnyösebb lenne, mint az azonnali műtét. Azonban csökkenteni akartam a vérnyomását, amíg a további PRP-t el nem lehetett végezni. A napi kétszer 500 mg Diamox néhány hétig, a műtétig biztonságos szinten tartotta a vérnyomását.
– Amikor a műtét nem jöhet szóba. Számos olyan betegem volt, akik nem reagáltak a helyi gyógyszeres vagy lézeres kezelésekre, de rettegtek a műtéttől. Egy 46 éves, 0,8-as csészével és korai látótérdefektussal rendelkező férfi betegnél egy héttel az argonlézeres trabeculoplasztika után (ritka helyzet) akut 50 mmHg-ra emelkedett az IOP; a Diamox sikeresen csökkentette a nyomását. Ekkor a beteg úgy döntött, hogy nem hajlandó a műtétre. Ehelyett, mivel minimális mellékhatásokat tapasztalt, a Diamox hosszú távú szedése mellett döntött.
– Amikor a helyi CAI nem jöhet szóba. A Neptazane enyhébb hatásával és csökkentett mellékhatásaival jó alternatíva, ha szükség van egy CAI hatására, de a beteg nem tolerálja a helyi CAI-kat, vagy egyszerűen csak jobban szereti a tablettákat, mint a cseppeket.
– A szürkehályogműtétet követő nyomásemelkedés megelőzésére. A fakoemulsifikáción átesett betegnél gyakran másnap nyomásemelkedés jelentkezik. Ezeknek a betegeknek a műtétet követő két étkezéskor két tabletta Diamox 500 mg-ot szedek, és a vérnyomásuk általában normális marad. (Ha másnap emelkedett vérnyomással jönnének be, akkor három nappal vagy egy héttel később kellene visszajönniük. Ez a profilaktikus kezelés kiküszöböli az extra látogatás szükségességét).
A szájon át alkalmazott CAI-k alkalmazása olyan rövid távú, hogy a betegeknél nem jelentkeznek mellékhatások. Nagyon ritka, hogy a beteg azzal jön be, hogy “bizseregnek az ujjaim.”
– A lézerkezelésre adott nyomásválasz tompítása. Néhány betegnél még mindig magas a nyomás annak ellenére, hogy már maximális gyógyszereket használnak, beleértve az Alphagant (brimonidin). Ez nem gyakori eset, de amikor ez előfordul, Diamoxot adok a betegnek, amikor előkészítik a lézerre, hogy az eljárás alatt a fedélzeten legyen. Ismétlem, az elszigetelt alkalmazással elkerülhetők a mellékhatásokkal kapcsolatos problémák.
– A betegek kezelésére, amikor a gyógyszerek helyi felszívódása nem megbízható. Ha a gyulladás súlyos vagy a szaruhártya ödémája kifejezett, a helyileg alkalmazott gyógyszerek felszívódása kevésbé megbízható. A súlyos szemfelszíni hegesedés szintén csökkentheti a helyileg alkalmazott gyógyszerek felszívódását. Ilyen helyzetekben a szisztémásan alkalmazott gyógyszerek megbízhatóbban szívódnak fel, és kivétel nélkül hatékonyabbak.
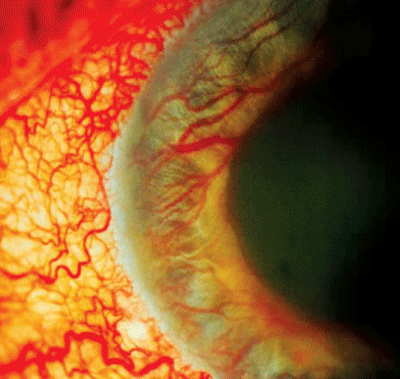
Egy neovaszkuláris glaukómás, proliferatív diabéteszes retinopátiás beteg, akinek a maximális helyi kezelés mellett 48 mmHg nyomás volt a jelöltje további panretinalis fotokoagulációra. A Diamox biztonságos szinten tartotta a nyomást, amíg további PRP-t nem lehetett végezni.
A dózist illetően a vizsgálatok szerint a Diamox 500 mg retard kapszula naponta egyszer vagy kétszer jobban tolerálható, mint a napi négy 250 mg-os tabletta.9 A Neptazane 25 vagy 50 mg-os tabletta naponta kétszer is bevehető; a magasabb dózis nagyjából egyenértékű a helyi CAI alkalmazásával. A Neptazane maximális ajánlott adagja 100 mg naponta háromszor. Általában mindkét gyógyszer csúcshatása körülbelül két órával a tabletták bevétele után, illetve nyolc órával az elnyújtott hatóanyag-leadású kapszulák bevétele után jelentkezik.
Mellékhatások kezelése
Amint fentebb említettem, számos páciensem választotta a szájon át szedhető CAI-k hosszú távú szedését, mert nem akarnak műtétet. Legtöbbjük arról számolt be, hogy nem nagyon zavarják őket a mellékhatások.
A szakirodalom mindazonáltal világossá teszi, hogy mellékhatások előfordulhatnak. A szemészeti mellékhatások közé tartozhat az idioszinkratikus, szulfonamiddal összefüggő átmeneti szögzáródás, rövidlátás és a chorioidea megvastagodása, de ezek ritkák, és (tapasztalataim szerint) nem olyanok, amelyek miatt aggódni kellene. A szisztémás hatások, beleértve a gyomor-bélrendszeri zavarokat, paresztéziát, diurézist, metabolikus acidózist, rossz közérzetet, étvágytalanságot, fémes ízt, az ujjak bizsergését és káliumkimerülést, gyakoribbak, különösen hosszan tartó alkalmazás esetén. (A káliumkimerülés valószínűbb, ha a beteg hidroklorotiazid-diuretikumot, digitalist vagy kortikoszteroidot is szed. Ilyen körülmények között a káliumszintet ellenőrizni kell). Súlyosabb reakciók, mint például vesekő, vérzészavarok vagy Stevens-Johnson-szindróma lehetségesek, de nagyon ritkák.
A Diamox és a Neptazane ellenjavallatai közé tartozik a szulfaallergia, illetve a vesekő vagy veseelégtelenség a kórtörténetben. Óvatosan kell eljárni, ha a beteg hajlamos a metabolikus acidózisra, törékeny cukorbeteg, májelégtelenségben szenved, vagy acidózissal járó krónikus obstruktív tüdőbetegségben szenved. Azt is fontos megjegyezni, hogy az egyidejű rendszeres aszpirinhasználat CAI-felhalmozódáshoz és toxicitáshoz vezethet.
Ha a mellékhatások lehetőségét minimalizálni szeretné, a Neptazane-t a legtöbb beteg jól tolerálja; ritkán okoz problémát a szisztémás hatásokkal. Nem szolgál azonban jól az IOP drámai csökkentésére. Jobb alternatíva lehet egy olyan beteg számára, akinek nehézséget okoz a cseppek használata, például egy idős, ízületi gyulladásban és remegésben szenvedő beteg számára. Nem túl gyakran ajánljuk betegeinknek.
A Diamox felírásakor természetesen figyelmeztetem a beteget a mellékhatások lehetőségére. A legtöbb esetben a felírás vagy egyszeri profilaktikus használatra, vagy néhány napos vagy hetes időtartamra szól. Ha arra számítok, hogy a műtétre váró páciens elég sokáig fogja szedni a gyógyszert ahhoz, hogy mellékhatásokat tapasztaljon, elmagyarázom, hogy ez egy rövid távú helyzet, amelynek célja, hogy megvédje a látását a beavatkozásig. Mondhatok valami olyasmit, hogy “nem szeretném, ha a műtétjét sürgősségi esetként végeznénk az éjszaka közepén, olyan asszisztens ápolókkal, akik nem ismerik az eljárást”. Néhány ilyen beteg olyan jól van, hogy végül inkább a tabletták szedése mellett dönt, mintsem a műtét elvégzése mellett.
Nem találkoztam a Diamoxhoz kapcsolódó súlyosabb mellékhatások egyikével sem, mint például vérzészavarok vagy aplasztikus anémia, annak ellenére, hogy viszonylag gyakran írtam fel. Biztos vagyok benne, hogy ez valószínűség kérdése, mert mindannyian tudjuk, hogy ilyenek előfordulnak. Azonban van 10 vagy 20 olyan betegem, akik évek óta szedik a Diamoxot incidens nélkül.
Az, hogy szükséges-e megfigyelni ezeket a betegeket, ha esetleg súlyosabb mellékhatások jelentkeznének, vita tárgyát képezi. Az éves találkozókon folytatott megbeszéléseken hallottam sebészektől azt az aggodalmat, hogy ha úgy döntenek, hogy rendszeresen megvizsgálják ezeknek a betegeknek a vérét, akkor valószínűleg gyakori hematológus segítségére lesz szükségük a határeseti eredmények értelmezéséhez. Emellett sok negatív tesztet végeznének annak érdekében, hogy megpróbáljanak azonosítani egy nagyon ritka állapotot, amelyet általában más tünetek alapján azonosítanak. Ez a helyzet végül idő- és fáradságköltséggel járhat minden érintett számára.
Nem hiszem, hogy a megfigyelésre szükség van, de több neves sebész nem ért egyet ezzel.
Az erőforrásokról szól
Amíg az orvostudomány folyamatosan fejlődik, és a régebbi alternatívákat újabb lehetőségek váltják fel, fontos, hogy ne tévesszük szem elől azokat az előnyöket, amelyekkel a régebbi lehetőségek még mindig rendelkeznek. Lehet, hogy az orális CAI-knak ma már nincs értelme a glaukóma első vonalbeli kezelésének, de még mindig értékes részét képezhetik a glaukómaorvos fegyvertárának.
Dr. Perkins a Madison-i Wisconsini Egyetem Szemészeti és Látástudományi Tanszékének docense.
1. Maus TL, Larsson LI, McLaren JW, Brubaker RF. A dorzolamid és az acetazolamid mint a vizes nedváramlás szupresszorainak összehasonlítása emberben. Arch Ophthalmol 1997;115:1:45-9.
2. McCannel CA, Heinrich SR, Brubaker RF. Az acetazolamid, de nem a timolol csökkenti a vizes nedváramlást alvó emberekben. Graefes Arch Clin Exp Ophthalmol. 1992;230:6:518-20.
3. Stewart WC, Halper LK, Johnson-Pratt L, Polis A, Hartenbaum D. A timololhoz adott dorzolamid versus acetazolamid tolerálhatósága és hatékonysága. J Ocul Pharmacol Ther 2002;18:3:211-20.
4. Hutzelmann JE, Polis AB, Michael AJ, Adamsons IA. A dorzolamid és az acetazolamid hatékonyságának és tolerálhatóságának összehasonlítása timolol kiegészítő terápiájaként. Oral to Topical CAI Study Group. Acta Ophthalmol Scand 1998;76:6:717-22.
5. Portellos M, Buckley EG, Freedman SF. Helyi kontra orális szénsavanyúság-gátló terápia gyermekkori glaukómában. J AAPOS 1998;2:1:43-7.
6. Centofanti M, Manni GL, Napoli D, Bucci MG. Szisztémás és lokális karbonátanhidráz-gátlók összehasonlító hatásai az intraokuláris nyomásra: klinikai maszkolt, cross-over vizsgálat. Pharmacol Res. 1997;35:5:481-5.
7. Gillies WE, Brooks AM. A dorzolamid vizsgálata glaukóma kezelésére. Ophthalmic Surg Lasers 1998;29:9:728-32.
8. Rosenberg LF, Krupin T, Tang LQ, Hong PH, Ruderman JM. Szisztémás acetazolamid és lokális dorzolamid kombinációja az intraokuláris nyomás és a vizenyőképződés csökkentésében. Ophthalmology 1998;105:1:88-92; vita 92-3.
9. Lichter PR, Newman LP, Wheeler NC, Beall OV. A betegek toleranciája a szénsav anhidráz gátlókkal szemben. Am J Ophthalmol 1978;85:4:495-502.