SONAL DESAI, ARCHITA PATEL AND S. Y. GABHE*
C. U. Shah College of Pharmacy, S. N. D. T. Women’s University, Sir Vithaldas Vidya Vihar, Juhu Tara Road, Santacruz (W), Mumbai – 400 049, India
Corresponding Authors: S. Y. GABHE E-mail:
| 受理日 | 16-Jan-2011 | ||
| 修正日 | 26-> | 16-Jan-2011 | 16-Jan-2011 |
| Date of Received | 9-Apr-2009 |
DOI.DO: 10.4103/0250-474X.89762
要旨
8-chlorotheophyllineのサンプル中に存在する3種の不純物を分離するために,シンプルなアイソクラティック逆相高速液体クロマトグラフィーを使用した。 不純物の特性評価にはLC-MSを使用した。 マススペクトルデータに基づき、これらの不純物の構造は、3,7-ジヒドロ-1,3-ジメチル-1H-プリン-2,6-ジオン(不純物I), 3,7-dihydro-1,3,7-trimethyl-1H-purine-2,6-dione (impurity II) and isomer of 8-chloro-1,3-dimethyl-2,6(3H,1H)-purinedione (impurity III) と特徴づけられることがわかった。
キーワード
8-Chlorotheophylline, impurity, LC-MS, reversed phase HPLC, theophylline
はじめに
原薬産業は特定品質の医薬品有効成分(API)の供給元としてすべての医薬品産業の基盤となっています。 原薬産業にとって大きな課題は、要求される品質と純度の最終医薬品を経済的に生産することである。 原薬の純度は、原料やその製造方法、晶析や精製プロセスの種類など、いくつかの要因に左右されます。 しかし、製造、精製、貯蔵のいずれにおいても不純物が混入するため、完全に純粋な原料を得ることはほとんど不可能である。 不純物とは、原薬に含まれる成分(水を除く)のうち、原薬として定義されている化学物質ではないものを指します。 ICHでは、化学合成により製造された原薬について、有機不純物、無機不純物、残留溶媒の3つのカテゴリーに分類しています。 不純物は、毒性があったり、物質の物理的・化学的性質を変化させ、薬として使えなくなる可能性がある。 不純物は製品の保存性を低下させ、製剤化を困難にする可能性がある。
ジメンヒドリネートやプロメタジンテオクレートのような抗ヒスタミン薬は、乗り物酔いの治療に広く使用されている薬物である。 8-クロロテオフィリンは、化学的には8-chloro-1,3-dimethyl-2,6(1H, 3H)- purinedioneで、これらの薬剤の塩形態の調製に使用される中間体であり、8-Chlorotheophyllineは、これらの薬剤の塩形態の調製に使用されています。 ジメンヒドリナートおよびプロメタジン テオクレートの純度および安全性を確保することが重要である。 そのためには、8-クロロテオフィリンを最高純度で、かつ不純物プロファイルが既知の状態で入手する必要があります。
文献調査から、Wadkeらは9-methylisoalloxazineと3,9-dimethylisoalloxazineと8-クロロテオフィリンの相互作用を研究していることがわかりました。 8-クロロテオフィリンは、HPLC法による尿酸塩の測定のための内部標準として使用されました。 また、電位差で測定した。 多成分製剤中のクロルフェノキサミン塩酸塩、8-クロロテオフィリンおよびカフェインの同時定量は、薄層クロマトグラフィー-電位差測定法で行った。 Gilらは、サイクリックボルタンメトリーと示差パルスポーラログラフィーにより8-chlorotheophyllineの電気分析挙動を調べ、示差パルスポーラログラフィーにより医薬品製剤中の含有量を定量した。 8-クロロテオフィリンとジフェンヒドラミンおよびカフェインについて、安定性を示すRP-HPLCメソッドを開発し、バリデートしました。 また、カフェイン、8-クロロテオフィリン、塩酸クロルフェノキサミンの三元混合物の同時測定のために、比スペクトルゼロ交差一次導関数分光光度法および化学量論的方法を開発した。 8-クロロテオフィリンに含まれる不純物の分離とキャラクタリゼーションのためのクロマトグラフィーおよび分光学的方法は、これまで報告されていない。 したがって、本研究は、現代の分析技術を使用して8-クロロテオフィリンに存在する不純物を分離し、特性評価することを目的として実施された
8-クロロテオフィリンはKores(インド)株式会社、サーンからの贈り物サンプルでした。 他のすべての化学物質と試薬は、S. D. Fine Chemicals Ltd (Mumbai, India) から調達した。 TLCおよび分取TLC研究に使用した溶媒は分析グレードであり、HPLC研究に使用した溶媒はHPLCグレードであった。 バッファーの調製には、ARグレードの酢酸ナトリウム三水和物を使用しました。
初めに、サンプル中に存在する不純物の数を知るために、TLC研究を実施しました。 固定相としてSilica gel 60GF254 (Merck)のプレコートTLCプレートを使用しました。 サンプルは最小量の酢酸エチルに溶解し、この溶液をTLCプレートのスポッティングに使用しました。 様々な移動相を試した。 酢酸エチル:トルエン:氷酢酸(10:0.3:0.5 v/v/v)は、他の移動相と比較して良好な分離を示しました。 8-クロロテオフィリン試料からTLCで4成分を分離し,Rf値はそれぞれ0.029, 0.132, 0.198, 0.852となりました。 8-クロロテオフィリンのRfは0.852でした。
TLC用の移動相を開発した後、分取TLCを用いて混合物を分離することを試みました。 試料は最小量の酢酸エチルに溶解し、バンド状にスポットした。 TLC試験で使用したのと同じクロマトグラフィー条件を用いて、3つの不純物すべてを分取TLCにより8-クロロテオフィリンから分離しました。 異なるバンドを別々に集め、酢酸エチルを用いて抽出した。 分離された不純物I、IIおよびIIIの量は非常に少なかったので、これらの不純物を一括して分離することに決定した。 不純物I、IIおよびIIIを総称してフラクションIとした。フラクションIは、分取TLCによって8-クロロテオフィリンから単離された。 各不純物が別々に分離されなかったため、IR、NMRなどの異なる識別技術を実施することができませんでした。 そこで、分離と同定を同時に行うことができるLC-MSを用いて、さらなる検討を行うことにしました。 LC-MS分析に先立ち、フラクションIのHPLCプロファイルが開発されました。 HPLC分析には、往復動ポンプCCPM、ポンプコントローラーPX8010、UV検出器を備えた東ソー高速液体クロマトグラフを使用した。 注入弁ユニットには、容量20μlのループを取り付けた。 フラクションIをアセトニトリルに溶解し、アセトニトリル:酢酸ナトリウム三水和物(pH 3.57; 0.01 M)(5:95v/v)からなる移動相で逆相HPLC分析に付した。 カラムはPhenomenex ODS (250×4.6 mm I.D.; 粒子径5 µm)を選択した。 流速は1.5 ml/minで、検出は波長280 nmでモニターした。 移動相は、使用前に真空下でG5焼結ガラスフィルターでろ過し、超音波処理して気泡を除去した。 フラクションIのHPLC分析でも、平均保持時間が8.324分、14.275分、20.933分の3つのピークが確認された(fig. 1)。 8356>
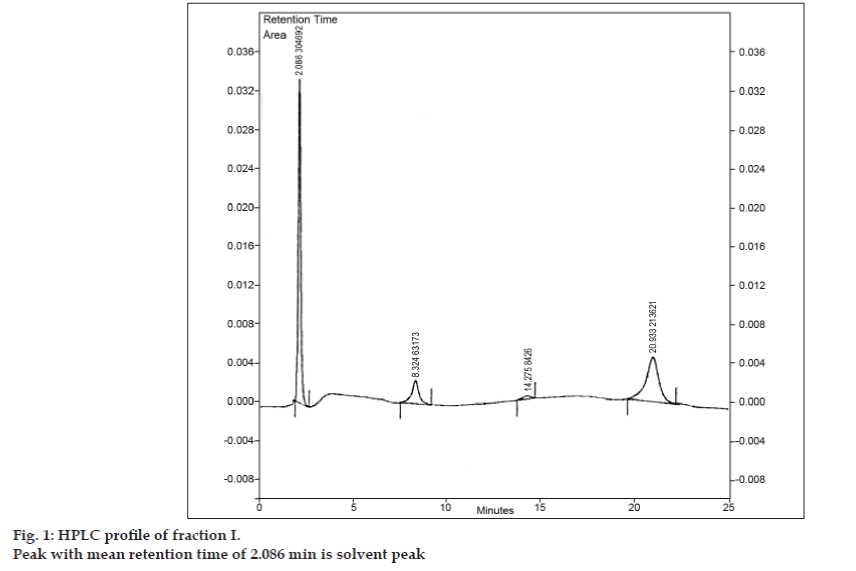
Figure 1: HPLC profile of fraction I.
Fraction I then subject to LC-MS analysis for characterization of impurities.平均保持時間が 2.086 min のピークは溶媒ピークでした。 LC-MS試験は、LC部が真空脱気装置(G1322A)、四重極ポンプ(G1311A)、オートサンプラー(G1313A)、UV/可視検出器(G1314A)からなる1100シリーズHPLC(Agilent Technologies, USA)、MS部がトリプル四重極質量分析計 Quattro II(Micromass UK Ltd.)からなるシステムで実施された。 8356>
LC-MS試験では、液体クロマトグラフィー分離はPhenomenex C18 column (250×4.6 mm, 5 µm) で、移動相はアセトニトリル:酢酸ナトリウムバッファ (5:95, v/v) で室温、流速は 1.5 ml/minで達成されました。 質量分析計は正電子スプレーイオン化(ESI)モードで、質量/電荷(m/z)比は120-500 m/zの範囲で動作させた。 ネブライジングガスには窒素を使用した。 データはMasslynxソフトウェアで取得・処理した。 不純物のマススペクトルデータが得られた (fig. 2, 3 and 4)。 3つのピークのフラグメンテーション経路は、メチル基および/またはカルボニル基の消失によって特徴付けられる。 180.9, 195.7, 214.9 の m/z 値を持つピークはそれぞれ +, +, + ピークに相当する。 得られたMSデータから、8.324分、14.275分、20.933分に溶出する不純物は、それぞれテオフィリン(mol.wt.180)、カフェイン(mol.wt.194)、8-クロロテオフィリンの異性体(mol.wt.214.5)でした(表 1)。 このように3つの不純物を分離し、マススペクトルデータからその構造を解明した(Scheme 1)。
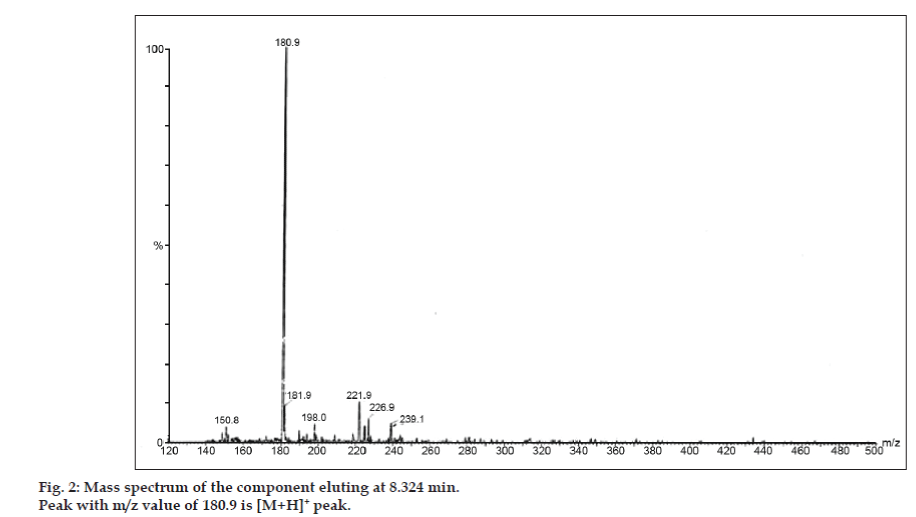
Fig. 2: 8.324 minで溶出する成分のマススペクトル
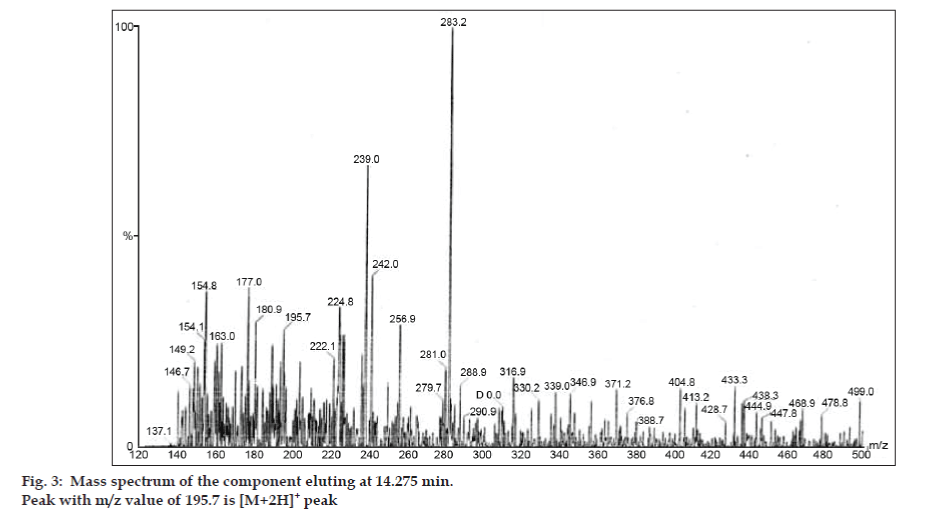
Fig.2:8分後に溶出する成分.Fig. 3: 14.275分に溶出する成分のマススペクトル
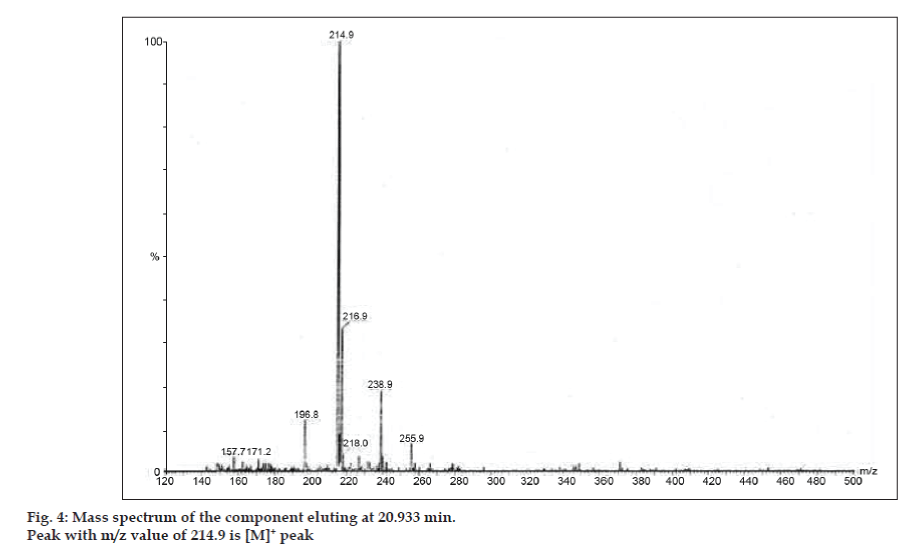
Figure. 4: 20.933 min.に溶出する成分のマススペクトル
| Peak no. |
保持時間(分) | フラグメントイオン(m/z) | 同定 |
|---|---|---|---|
| 8.324 | 181.9 +, 180.9 +, 150.8 + | Theophylline | |
| 14.275 | 195.7 +, 180.9 +,149.2 +, 137.1+ | Caffeine | |
| 216.1 +,176.1 +,176.2 +,176.1 +,176.1 +,176.1 +,176.1 +,186.3 | Caffeine9 +, 214.9 +, 171.2 +, 157.7 + | 8- Chlorotheophylline |
TABLE 1のアイソマー。 HPLC-MS IDENTIFICATION OF FRACTION I
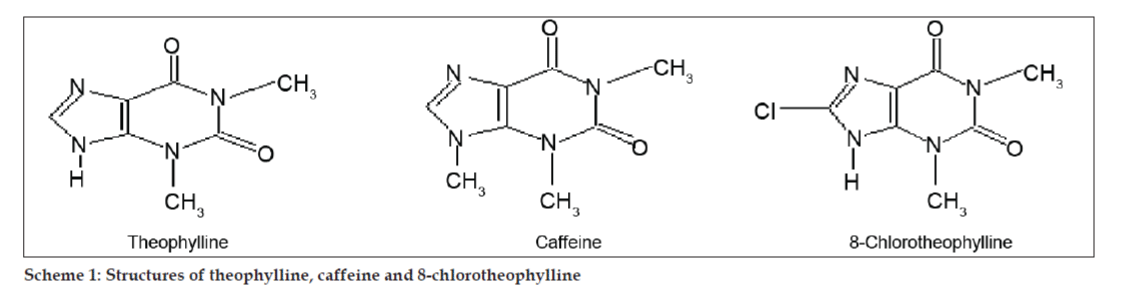
スキーム1:テオフィリン、カフェインおよび8-chlorotheophyllineの構造
Acknowledgements
著者はKores (India) Ltd.に感謝しています。 8356>
- Kasture AV, Wadodkar SG, Mahadik KR, More HV.による8-クロロテオフィリンのギフトサンプルの提供に感謝します。 医薬品分析. Vol.1. プネー NiraliPrakashan; 1997. p. 12-4.
- United State Pharmacopoeia, Vol.26. Rockville, MD: United States Pharmacopoeia Convention, Inc.; 1999. p. 2049-59.
- Ahuja S, Alsante KM. 医薬品中の不純物の分離と特性評価ハンドブック(Handbook of isolation and characterization of impurities in pharmaceuticals). California:
- Foye WO, Lemke TL, Williams DA.東京大学出版会; 2003.p.6. メディシナルケミストリーの原理。 第4版. ニューデリー: B. I. ウェーバリー社; 1995. p. 419.
- Reynolds JE. マーチンデール-ザ・エクストラ・ファーマコペア. 29th ed. ロンドン。 Pharmaceutical Press; 1989. p. 451,459.
- Wadke DA, Guttman DE. 反応速度に対する錯体形成の影響 III. スペクトル、溶解度、速度論的方法によるいくつかのiso-alloxazinesと8-chlorotheophyllineの相互作用。 J Pharm Sci 1965;54:1293.
- Bennett MJ, Patchett BP, Worthy E. A simple HPLC method for the determination of urate in serum and urine using 8-chlorotheophylline as internal standard. Med Lab Sci 1984;41:108-11.
- Nikolic K, Medenica M. 8-chlorotheophyllineの電位差定量. マイクロキミカ・アクタ 1986;88:5.
- Bebawy LI, El-Kousy NM. 薄層クロマトグラフィー濃度測定法による多成分製剤の同時定量。 J Pharm Biomed Anal 1999;20:663-70.
- Gil EP, Blazquez LC, Garcia-MoncoCarra RM, Misiego AS. 8-クロロテオフィリンのポーラログラフ挙動と製剤中の定量. Electroanalysis 1993;5:343.
- Barbas C, Garcia A, Saavedra L, Castro M. isocratic high performance liquid chromatographyによるカフェイン、8-クロロテオフィリン、ジフェンヒドラミンの定量法の最適化とバリデーション Stress test for stability evaluation.Coming a method for quantitative of the caffeine, 8-chlorotheophylline isocratic high performance liquid chromatography by the dishenhydramine. J ChromatogrA 2000;870:97-103.
- Kelani KM. 比スペクトルゼロ交差一次導関数分光光度法およびケモメトリック法による三元混合物中のカフェイン、8-クロロテオフィリンおよび塩酸クロルフェノキサミンの同時定量。 J AOAC Int 2005;88:1126-34.
.